Антиретровирусная терапия и ее влияние на здоровье пациентов с ВИЧ
Несмотря на прогресс современной медицины в лечении и профилактике ВИЧ-инфекции, по оценкам ВОЗ, в конце 2012 года в мире насчитывалось 35,3 миллиона людей с ВИЧ, из которых 2,3 миллиона составляли случаи новых заражений. Кроме того, более 1 миллиона людей в год умирает от осложнений, связанных с ВИЧ (1). Наиболее быстро ВИЧ распространяется в Восточной Европе, и заболеваемость в Украине остается на достаточно высоком уровне. Именно поэтому главной целью ВОЗ является оптимизация профилактики передачи этого заболевания и существующих методов терапии, а также обеспечение своевременного контроля действенности терапии, минимизации побочных эффектов и повышению, таким образом, общей эффективности лечения(1).
Как действует ВИЧ?
ВИЧ поражает иммунокомпетентные клетки – CD4+-Т-лимфоциты, имеющие также название — «хелперы» (от английского слова «help» –помогать). Именно эта популяция лимфоцитов, несущих на поверхности рецепторы CD4, отвечает на клеточном уровне за иммунный ответ — способность организма эффективно противостоять инфекциям. Вирус постепенно инфицирует все большее и большее количество CD4+-Т-лимфоцитов, а инфицированные ВИЧ клетки гибнут. Соответственно, число CD4+-Т-лимфоцитов в организме снижается, что приводит к нарушению сначала клеточного иммунитета, а потом гуморального иммунного ответа (выработки антител, связывающих чужеродные агенты при их попадании в организм). Далее вирус поражает и другие типы клеток, например, макрофаги, отвечающие за «обезвреживание» инородных агентов, попадающих в организм. В результате нарушается связь между различными типами клеток, лежащая в основе иммунного ответа. Нарастает поражение иммунной системы, которое приводит к заражению больного сопутствующими ВИЧ ( т.н. оппортунистическими) инфекциями – туберкулезом, токсоплазмозом, гепатитом В и другими опасными заболеваниями. На более поздних этапах поражение иммунной системы приводит к развитию злокачественных новообразований и к синдрому приобретенного иммунодефицита (СПИДу) — последней стадии заболевания. При отсутствии лечения у большинства ВИЧ-инфицированных людей пациентов от момента постановки диагноза ВИЧ до развития СПИДа проходит примерно10-15лет(3).
Можно ли вылечить ВИЧ?
Основная сложность борьбы с ВИЧ заключается в сильной изменчивости протеинов (белков), входящих в состав оболочки вируса, из-за которых иммунитет не в состоянии выработать антитела, способные блокировать вирус на выходе из клетки и предотвратить дальнейшее его распространение и гибель популяции Т-лимфоцитов. Поэтому на сегодняшний день не существует лекарства, способного полностью излечить заболевание, хотя достижения современной медицины позволяют надеяться на то, что мир стоит на пороге открытия способа терапии, позволяющего обеспечить полное выздоровление пациента. В 2013г в американском штате Миссисипи был официально зарегистрирован уникальный случай девочки 2,5 лет, которой удалось выздороветь сразу после агрессивного курса лечения, проведенного вскоре после рождения. А ученым Орегонского университета удалось добиться успеха при исследованиях вакцины против ВИЧ на животных – если в 1 фазе исследования препарат помог всего 50% инфицированных обезьян, то во 2 фазе полностью избавились от вируса практически 100% животных. Это говорит о том, что в перспективе возможен путь обезвреживания вируса на том этапе, когда он еще находится в клетке.
Однако на сегодняшний день, когда средства, позволяющего полностью вылечить ВИЧ, не существует, ключевым фактором, от которого зависит прогноз заболевания, является своевременное начало антиретровирусной терапии, которая может практически полностью остановить прогрессирование заболевания и предотвращает дальнейшую передачу вируса (1).
Что такое антиретровирусная терапия (АРТ)?
Антиретровирусные препараты направлены на замедление репродукцию вируса, т.е. на уменьшение его количества в организме. Антиретровирусная терапия (АРТ) существенно замедляет прогресс заболевания именно путем предотвращения репликации вируса и, следовательно, уменьшение концентрации вирусной РНК (известной как «вирусная нагрузка»,или «виремия») в крови пациента. В конце 2012 года антиретровирусную терапию получало 9,7 миллиона человек в странах с низким и средним уровнем дохода. По рекомендации ВОЗ, она применяется лишь после всех необходимых тестов и время ее начала определяет индивидуально лечащий врач (1). Показания к антиретровирусной терапии и оценка ее эффективности основаны на регулярном определении концентрации вирусной РНК (количественном определении РНК ВИЧ) и уровня лимфоцитов CD4. Снижение концентрации вирусной РНК в крови ведет к повышению уровня лимфоцитов CD4 и отдалению развития СПИДа.
Когда следует начинать АРТ?
Независимо от стадии заболевания, АРТ следует назначать всем пациентам, у которых уровень лимфоцитов CD4 составляет >350 клеток/мм3 и ≤ 500 клеток/мм3. АРТ также следует назначать всем пациентам, у которых уровень лимфоцитов CD4 составляет ≤350 клеток/мм
Какие препараты назначаются в составе АРТ?
Высокоактивная антиретровирусная терапия, согласно рекомендациям ВОЗ 2013г, состоит из одновременного приема трех-четырех сильнодействующих препаратов. Существует три группы антиретровирусных препаратов: нуклеозидные ингибиторы обратной транскриптазы (НИОТ), ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) и ингибиторы протеазы (ИП)(2).
Согласно рекомендациям ВОЗ, в качестве первой линии АРТ при ВИЧ-инфекции назначаются два препарата НИОТ и один – ННИОТ (тенофовир (TDF) + ламивудин (3TC) или эмтрицитабин (FTC) + эфавиренз (EFV) в фиксированных дозах; при непереносимости данной комбинации, ее недоступности на рынке или противопоказаниях к ней назначаются зидовудин (AZT) + 3TC + EFV, или AZT + 3TC + невирапин (NVP),или TDF + 3TC (or FTC) + NVP.Использование ставудина (d4T) в качестве терапии первой линии не рекомендуется ввиду его серьезных побочных эффектов. В качестве терапии второй линии рекомендуется комбинация двух НИОТ и ИП, усиленных ритонавиром. Общие принципы перехода на терапию второй линии, как и в случае терапии первой линии, основываются на комбинации двух НИОТ в фиксированных дозах: если схема TDF + 3TC (или FTC) оказалась неэффективной, следует использовать схему, основанную на зидовудине и ламивудине (AZT + 3TC), а если эта схема, или схема, основанная на ставудине, при ее применении в качестве терапии первой линии, оказалась неэффективной, то наоборот, следует заменить ее на схему TDF + 3TC (или FTC).Из ингибиторов протеазы рекомендуются атазанавир (ATV) и лопанавир (LPV) в фиксированных дозах. Наконец, режимы терапии третьей линии ВОЗ рекомендует регламентировать национальными протоколами, включая в них препараты с минимальным риском перекрестной резистентности ( устойчивости) вируса к тем препаратам,что уже использовались в схемах терапии первой и второй линии у данных пациентов, если по каким-либо причинам эти схемы пришлось отменить ( из-за плохой переносимости, неэффективности, выраженности побочных эффектов).
Эффективность терапии определяется с помощью клинических исследований через 6-12 месяцев после ее начала. Наиболее достоверным является определение уровня РНК вируса в крови (вирусной нагрузки), но если этот тест не доступен, используется обыкновенное измерение уровня лимфоцитов CD4,по которому можно судить о прогрессе заболевания и эффективности применяемой схемы(2).
Почему соблюдение режима АРТ имеет решающее значение для дальнейшего прогноза пациента?
По данным разных источников, до 50% носителей ВИЧ после двух-трех лет лечения отказываются от терапии, тем самым обрекая себя на скорый прогресс заболевания и ухудшение качества жизни(4). Важно понимать, что лечение ВИЧ является пожизненным, которое нельзя прекращать – иначе возобновление жизненного цикла вируса, который «поднимет голову» вскоре после прекращения терапии, приведет к началу нового витка гибели иммунокомпетентных клеток, ухудшению состояния иммунитета, присоединению новых инфекций и прогрессу заболевания вплоть до развития СПИДа. На самом деле терапия ВИЧ не требует особых изменений в привычном режиме пациента – препараты АРТ обычно принимают один или два раза в день, и пациенты, у которых правильно подобрана схема терапии, очень быстро отлаживают режим их приема. Он ничем не отличается от режимов приема препаратов, принимаемых «здоровой» частью населения – людьми с диабетом, с заболеваниями щитовидной железы, с сердечно-сосудистыми заболеваниями, а иногда и оказывается значительно более простым — недаром пациенты с многолетней историей приема АРТ часто говорят, что пьют эти таблетки, как витамины.
Нельзя пропускать прием таблеток или «забывать» о следующей дозе более чем на 2 часа после стандартного времени приема – статистика показывает, что АРТ эффективна тогда, когда пациент принимает не менее 95% от необходимой дозы всех препаратов(4), что означает, что при приеме 1 раз в день в месяц можно пропустить всего лишь прием одной дозы, а при приеме 2 раза в день – не более 3 приемов!
Кроме того, необходимо помнить о возможных лекарственных взаимодействиях компонентов АРТ с другими принимаемым пациентом лекарственными препаратами. Иногда последние могут усиливать эффект АРТ, а иногда, наоборот, его уменьшать. Эффект лекарственных взаимодействий зависит от фармакокинетики дополнительно принимаемых пациентом препаратов — скорости достижения максимальной концентрации в крови, периода полувыведения, всасываемости в кишечнике. Поэтому не следует начинать прием никаких дополнительных лекарственных средств на фоне АРТ без консультации с врачом-инфекционистом. Даже при приеме обезбаливающих препаратов или растительных средств (фитотерапии) следует предварительно получить консультацию врача. Особенно часто во взаимодействие с другими препаратами вступают ИП и НИОТ. Их действие может ослабевать под действием препаратов, принимаемых для снижения кислотности желудочного сока (например, ингибиторы протонной помпы) или некоторых антибиотиков (макролидов). И наоборот, обычный грейпфрутовый сок может многократно увеличивать эффективность некоторых ИТ (4). Наблюдается также и «обратное» влияние – лекарства, применяемые для АРТ могут снижать эффективность , например, некоторых гормональных препаратов, противозачаточных средств, — последние под влиянием АРТ очень быстро выводятся из организма,- поэтому женщинам, принимающим АРТ, рекомендуется использовать дополнительные методы контрацепции. Некоторые сильнодействующие обезболивающие из группы опиоидов (метадон) также вступают во взаимодействие с препаратами АРТ, вследствие чего может потребоваться увеличение их доз.
Отдельно следует отметить препараты, снижающие уровень холестерин (ХС) в крови(статины), которые некоторые пациенты принимают постоянно. Учитывая, что одним из побочных действий АРТ является увеличение уровня ХС, а также других составляющих т.н. «липидного профиля» ( например, триглицеридов (ТГ), логично предположить, что на фоне АРТ продолжение приема статинов благоприятствует общему состоянию здоровья пациента, снижая уровень ХС. Однако поскольку в организме и статины и препараты АРТ метаболизируются одним и тем же путем, их одновременное применение способствует усилению опасного побочного эффекта статинов – разрушения мышц, или рабдомиолиза. Поэтому при одновременном приеме статинов и препаратов АРТ обязательно необходимо проконсультироваться с врачом.
При приеме препаратов АРТ не следует верить и в распространенный миф о том, что постоянный прием таблеток от ВИЧ вреден и сопряжен с необратимыми токсическими эффектами. Терапия ВИЧ действительно имеет побочные действия, которые, тем не менее, можно минимизировать, а часто и свести к нулю, если соблюдать рекомендации по лечению и проходить необходимые обследования, чтобы врач мог вовремя сориентироваться, какие органы и системы пациента наиболее чувствительны к назначенным препаратам, и купировать имеющиеся нежелательные симптомы.
Какими побочными эффектами обладает АРТ?
Побочные эффекты АРТ делят на т.н. «ранние» и «поздние»( 4). К «ранним» эффектам относят такие, как понос, тошнота, рвота, жажда, боль в животе, усталость, бессонница, выпадание волос, диспепсия. Иногда могут наблюдаться также изменения в системе кроветворения, определяемые путем простейших исследований, например, общего анализа крови (уменьшение числа нейтрофилов, или нейтропения) или биохимических исследований (повышение уровня АЛТ, АСТ ( «печеночные пробы»). Следует помнить, что все эти побочные явления могут быть кратковременными, а также то, что их возникновение ассоциируется не с АРТ в целом, а с приемом определенного препарата определенной группы (НИОТ ,ИП).
К «поздним» эффектам АРТ относят те нежелательные явления, которые могут возникать по прошествии многих месяцев или лет приема препарата. К наиболее серьезным из них относятся нарушения углеводного обмена (повышение уровня сахара в крови, вплоть до развития диабета) и изменения липидного (жирового) обмена. Эти изменения очень важно вовремя диагностировать, поскольку, в отличие от «ранних» эффектов, они могут оставаться незамеченными пациентом, и, будучи нелеченными, увеличивать риск сердечно-сосудистых заболеваний, вплоть до инфаркта.
Современная медицина располагает всеми средствами, чтобы препятствовать развитию «поздних» побочных эффектов АРТ. Самым «заметным» из них является липодистрофия, или истощение жировой ткани на фоне АРТ, ассоциирующиеся с нарушениями липидного обмена и изменениями липидного профиля пациентов(5). Данные крупных исследований показывают, что наличие липодистрофии и повышение уровня CD4+-Т-лимфоцитов у пациентов с ВИЧ имеет сильную корреляцию с увеличением риска сердечно-сосудистых событий (инфаркта)(5). Помимо этого, липодистрофия очень часто сопряжена с нарушениями липидного обмена – возрастанием уровня ХС засчет роста уровня липопротеинов низкой плотности (ЛПНП) и ТГ. Особенно часто рост уровня ХС и ТГ наблюдается у пациентов, получающих терапию ИП, усиленную ритонавиром. Поэтому одной из основных рекомендаций для пациентов, получающих ИП, является регулярный контроль показателей липидного обмена (липидограмма). За 8-12 часов до проведения этого исследования, для которого у пациента берется кровь из вены натощак, не следует есть ничего жирного, а еще лучше – не есть вообще, чтобы получить точные результаты(4). Точность результатов липидограммы у пациентов с ВИЧ приобретает первостепенное значение, поскольку нарушения липидного обмена важно диагностировать на той стадии, пока препараты АРТ не привели к выраженным нарушениям. На начальных стадиях часто эффективными оказываются изменение образа жизни и соблюдение диеты, рекомендуемой для снижения уровня ХС (антиатеросклеротическая диета), а также умеренная физическая нагрузка. Однако при неэффективности указанных мер, пациенту могут быть назначены препараты, снижающие уровень ХС и ТГ в крови – статины. Как уже упоминалось, некоторые из них вступают во взаимодействие с компонентами АРТ, поэтому назначение кардиолога следует согласовывать с лечащим инфекционистом.
Наконец, такой нежелательный поздний эффект препаратов АРТ, как рост уровня сахара в крови, легко можно купировать на начальных стадиях, пока повышенным оказывается только уровень глюкозы натощак — с помощью диеты и изменения образа жизни. Гораздо сложнее это сделать потом, когда нарушения углеводного обмена нарастают и доходит даже у развития пациента диабета 2 типа.
Именно поэтому для пациентов, получающих АРТ-терапию, первостепенное значение имеет регулярный контроль показателей углеводного (уровень сахара в крови натощак) и липидного ( уровень общего ХС и триглицеридов, а при необходимости – более расширенное исследование, т.н. липидограмма)(4). В некоторых регионах (например, на африканском континенте) такие исследования рекомендуют в качестве рутинного скрининга для всех пациентов с ВИЧ – инфекцией, как эффективное средство снижения риска ССЗ(6).
Может ли АРТ-терапия обеспечить качество жизни пациентов?
Хотя на сегодняшний день АРТ-терапия не обеспечивает полного излечения пациента, она может существенно увеличить его продолжительность жизни без ущерба для ее качества(4). Очень важно своевременно, после подтверждения диагноза, начать одну из рекомендованных ВОЗ схем терапии и тщательно ее придерживаться, сообщая лечащему врачу обо всех побочных эффектах, самочувствии на фоне терапии, дополнительно принимаемых препаратах, а также проходить назначенные обследования. Регулярное измерения уровня вирусной нагрузки и\или CD4+-лимфоцитов позволяет сделать выводы об эффективности лечения, а регулярный контроль углеводного (сахар крови) и липидного ( ХС, ТГ) обмена позволит вовремя предотвратить нежелательные побочные эффекты АРТ-терапии на организм. При правильном подборе АРТ-терапии, соблюдении рекомендаций врача и регулярных контрольных обследованиях она гарантирует пациенту долгую и полноценную жизнь, ничем не уступающую жизни здорового пациента по качеству.
Список литературы:
- Всемирная Организация Здравоохранения (ВОЗ). ВИЧ/СПИД. Информационный бюллетень № 360. Октябрь 2013.
- World Health Organization. Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection: recommendations for a public health approach. Geneva: World Health Organization; 2013.
- Терапевтический справочник Вашингтонского университета. Москва ,200.с 388-404.
- Elżbieta Bąkowska, Dorota Rogowska—Szadkowska. LECZENIE ANTYRETROWIRUSOWE (ARV) . Materiały informacyjne dla osób żyjących z HIV. Krajowe Centrum ds.AIDS, Polska, 2007.
- De Socio GV et al. CISAI study group. Identifying HIV patients with an unfavorable cardiovascular risk profile in the clinical practice: results from the SIMONE study. J Infect. 2008 Jul;57(1):33-40.
- Ssinabulya I et al. Subclinical atherosclerosis among HIV-infected adults attending HIV/AIDS care at two large ambulatory HIV clinics in Uganda. PLoS One. 2014 Feb 28;9(2)
Читайте также
www.health-ua.org
Побочными эффектами терапии от ВИЧ-инфекции.
Профессиональное лечение наркомании и алкоголизма!
Мы сотрудничаем с наркологическими центрами по всей стране!
Позвоните прямо сейчас!
8 800 551 50 95
У каждого противовирусного препарата может быть побочное действие, но это же относится к абсолютно любому лекарству. Все очень индивидуально, и если в инструкции к препарату вы видите длинный список побочных эффектов, то это не значит, что у вас обязательно появится хотя бы один из них. Некоторые не испытывают никаких побочных эффектов от терапии, другие испытывают их в мягкой форме, не осложняющей жизнь, у кого-то побочные действия могут быть тяжелыми.
Главное правило
Ключевой момент в борьбе с возможными побочными эффектами: заранее знать, чего можно ожидать и иметь готовый план действий в случае появления того или иного побочного действия. Если вы собираетесь принимать препарат, у которого есть хотя бы небольшая вероятность опасных побочных действий, вы должны заранее знать симптомы, на которые вам нужно обратить внимание. Также возможно уменьшить симптомы с помощью специальных профилактических действий. Прежде чем начинать пить терапию обсудите с врачом возможный риск, связанный с препаратами.
Половой вопрос
Реакции женщин на самые различные лекарства могут отличаться от мужчин. До сих пор не до конца ясно, почему это происходит. Возможно, что тому виной различие в массе тела или в половых гормонах. Как бы там ни было, женщинам необходима новейшая информация о побочных эффектах именно среди женщин.
За чем следить и что делать?
Когда люди только начинают принимать противовирусную терапию, им обычно становится хуже, а не лучше. Это нормально, и бояться этого не следует. Подавляющее большинство побочных действий исчезают через 4-6 недель после начала приема терапии. Этот период необходим, чтобы организм адаптировался к новым лекарствам. До того как это произойдет, люди могут испытывать головную и мышечную боль, головокружение и тошноту. Как только тело привыкнет, эти побочные эффекты должны исчезнуть.
Необходимо учиться распознавать нежелательные действия, как только они появляются. К большинству побочек можно приспособится. В других случаях, побочные действия могут быть сигналом для обращения за медицинской помощью. После начала приема терапии сообщайте врачу обо всех непривычных для вас реакциях. Если это возможно, постарайтесь поговорить с людьми, которые принимали такой же препарат. Вполне возможно, что они сталкивались с той же проблемой и уже нашли решение.
Все кажется сложным поначалу
Очень часто люди принимают за побочные эффекты симптомы тревоги, стресса и депрессии. Позаботьтесь о себе в ЦЕЛОМ, включая свои эмоции, свои мысли о здоровье, а также стратегию по борьбе с ВИЧ — это позволит вам уменьшить негативные чувства и их последствия.
Период привыкания к лекарствам можно сделать проще и спокойнее. Постарайтесь заранее разгрузить свое расписание и не планируйте на это время серьезных дел и большого объема работы. Если у вас обычно слишком много забот, попросите кого-нибудь о помощи, например по дому или в присмотре за детьми.
В это время на первом месте должно быть ваше здоровье. Старайтесь побольше спать и отдыхать. Питайтесь правильно, с учетом возможной тошноты или диареи. Постарайтесь каждый день делать физические упражнения — хотя бы выходить на прогулку.
В этот период вам особенно нужна поддержка семьи, друзей или группы взаимопомощи. Если вы можете, расскажите им о том, что с вами происходит. Иногда простой разговор помогает, но также вам могут подать хорошую идею по облегчению побочных действий, о которой ваш врач даже не упоминал.
Кое-что о смене препаратов
Иногда люди испытывают действительно серьезные побочные эффекты, из-за которых они могут захотеть сменить режим терапии на другой, даже если их лекарства хорошо контролируют ВИЧ.
Замена препарата исключительно по причине побочных действий также позволит «приберечь» этот препарат на будущее в случае провала текущей комбинации. Тем более, что испытываемые вами сейчас побочные эффекты могут не повториться, если вы попробуете это лекарство в будущем.
Однако, следует помнить о том, что просто перестать пить тот или иной препарат очень опасно. Также опасно уменьшать дозу лекарства, не посоветовавшись со своим врачом. Это может привести к развитию резистентности к этому препарату, а возможно, и к другим препаратам этого класса.
Бок о бок с побочками
Побочные эффекты очень часто появляются после начала приема противовирусной терапии, но через несколько недель они уменьшаются или исчезают совсем. Иногда они могут продолжаться в течение всего приема комбинации, но даже в этом случае их можно минимализировать и многие люди решают продолжить прием терапии, несмотря на симптомы.
Большинство симптомов, связанных с препаратами, похожи на заболевания, с которыми люди имели дело и раньше, например, гормональные нарушения, беременность, депрессию или саму ВИЧ-инфекцию. Что бы ни беспокоило человека, очень важно обсудить это с врачом и диагностировать причину недомогания.
Ниже приведены краткие рекомендации для борьбы с наиболее распространенными побочными эффектами.
Хроническая усталость
Все мы чувствуем усталость время от времени, но если усталость продолжается постоянно, независимо от обстоятельств — то это медицинская проблема. Если ее игнорировать, она может ухудшиться.
Симптомы усталости могут быть физическими. Например, трудности при утреннем подъеме или при ходьбе по лестнице. Они могут быть психологическими. Например, неспособность концентрировать на чем-то внимание. Хроническая усталость может иметь массу возможных причин, которые не всегда можно сразу диагностировать.
Первый шаг в борьбе с хронической усталостью — это распознать ее. Если вы чувствуете постоянную усталость, спросите себя: Как быстро вы устаете? Трудно ли вам делать что-то, с чем не возникало проблем пару месяцев назад? Легко ли вам сконцентрироваться на чем-то? Нормально ли вы спите? Чем больше информации о своем физическом и психологическом состоянии вы предоставите врачу, тем проще будет найти средство от вашего состояния.
Рекомендации
– Старайтесь ложиться и вставать в одно и то же время. Изменения в распорядке сна могут вызвать усталость.
– Попытайтесь хотя бы немного поупражняться физически. Это уменьшит стресс и поможет вам чувствовать себя сильнее.
– Покупайте побольше готовых продуктов, чтобы избавить себя от необходимости готовить.
Анемия
Анемия — это потеря красных кровяных клеток. При анемии тканям организма не хватает кислорода, что вызывает чувство усталости и потери сил. У женщин симптомом анемии могут быть нарушения месячного цикла. В некоторых случаях анемия опасна для здоровья. У большинства людей с ВИЧ бывает анемия в те или иные моменты жизни.
Иногда причина бывает в самой ВИЧ-инфекции, в других случаях анемию могут вызвать некоторые противовирусные препараты, например ретровир.
Чтобы вовремя диагностировать анемию необходимо следить за количеством красных телец. Изменения в питании и специальные пищевые добавки уменьшают риск анемии. Также существуют специальные лекарства для ее лечения. В самых худших случаях необходимо прекратить прием препаратов и изменить комбинацию.
Рекомендации
– Регулярно проверяйтесь на количество красных кровяных телец (гемоглобин).
– Рыба, мясо и птица богаты железом и витамином В-12. Оба они снижают риск анемии.
– Шпинат, салат, спаржа, зеленый горошек богаты фолиевой кислотой, которая также полезна для профилактики анемии.
Головная боль
Основная причина головной боли — это напряжение, которое все мы можем испытывать. Тем не менее, некоторые лекарства, включая противовирусные, могут вызывать ее. Существует множество лекарств от головной боли. Кроме того, ее можно уменьшить, если уменьшить стресс.
Рекомендации
– Попробуйте отдохнуть в комнате, где темно и тихо, закройте глаза.
– Положите на глаза холодный компресс, аккуратно помассируйте скулы, примите горячую ванну.
– Чтобы предотвратить головную боль, постарайтесь узнать, что ее может спровоцировать. Избегайте еды, которая может ее вызвать, особенно кофеина (он содержится в кофе, чае и коле), шоколада, вина, цитрусовых, пищевых добавок, сыра, лука и уксуса.
Тошнота и рвота
Некоторые из противовирусных препаратов потенциально могут вызвать тошноту у некоторых людей. Если у вас появилась рвота, тем более если она стала хронической, то необходимо срочно связаться с врачом, тем более, что она может помешать принимать препараты.
Рекомендации
– Включите в рацион бананы, рис, яблочный сок и поджаренный хлеб.
– Оставляйте рядом с кроватью какие-нибудь сухие крекеры или хлебцы. Прежде чем вставать, съешьте парочку и посидите немного в кровати. Это поможет бороться с утренней тошнотой.
– Попробуйте чай из мяты, ромашки или имбиря. Они могут успокаивать желудок.
– Избегайте горячей, острой, сильно пахнущей и жирной пищи.
– Поговорите с врачом о возможности назначения препаратов против тошноты.
Диарея
Хроническая диарея может привести к обезвоживанию, поэтому в этом случае необходимо стараться пить как можно больше жидкости, а также полноценно питаться. Существует множество очень хороших препаратов против диареи. Если ваши лекарства могут ее вызвать, поговорите с врачом о назначении таких препаратов заранее.
Рекомендации
– Ешьте побольше бананов, вареного риса, яблочного сока, каш и хлеба (незернового) — это прекрасное домашнее средство от диареи.
– Избегайте продуктов с нерастворимой клетчаткой, например фруктов и овощей с кожицей. Они могут ухудшить диарею.
– Старайтесь избегать жирной или очень сладкой пищи.
– Принимайте кальций (500 мг дважды в день).
– Пейте побольше жидкости, чтобы предотвратить обезвоживание.
Сухость во рту
Сухость во рту может появиться в результате приема некоторых препаратов. Главное лечение в этом случае — обильное питье и по возможности отказ от сладкой еды и кофеина. «Жевательные резинки без сахара» — это хороший способ преодолеть сухость. Если это не помогает, необходимо посоветоваться с врачом о назначении специальных лекарств.
Рекомендации
– Регулярно полощите рот теплой водой.
– Попробуйте пососать леденец без сахара, лед, или пожевать жвачку.
– Попросите врача назначить полоскание для рта или специальные лекарства.
Сыпь
По непонятным пока причинам, сыпь тяжелее проходит у женщин, принимающих противовирусные препараты, чем у мужчин. Обычно сыпь появляется у людей принимающих невирапин или нелфинавир. Очень важно следить за состоянием кожи, особенно после назначения нового препарата, и срочно обращаться к врачу в случае каких-то симптомов.
Рекомендации
– По возможности замените мыло другими очищающими средствами, используйте нейтральное мыло без запаха.
– Избегайте лишних ванн и душей, они раздражают кожу.
– Постарайтесь не загорать и избегать солнечного ультрафиолета, он может ухудшить проявления сыпи.
– Заранее приобретите лекарство против сыпи, смягчающее кожу и держите его под рукой.
www.aids.ru
www.hiv-sar.ru
Препараты для лечения ВИЧ и СПИДА
Лучшие препараты для лечения СПИДА способны замедлить развитие болезни, и продлить жизнь пациента. Лекарства не приведут к полному выздоровлению, зато позволят предупредить ухудшение.
Существует несколько основных видов терапии:
- антиретровирусная
- патогенентическое лечение
- профилактика инфекций (паразитарных, вирусных, бактериальных и др.)
Три группы средств доказали свою действенность и активно применяются в современных условиях. Это ингибиторы протеазы вируса иммунодефицита, ингибиторы обратной транскриптазы, являющиеся аналогами нуклеозидов и ненуклеозидные препараты, ингибирующие данный фермент.
К первой группе относятся Агенераза, Реатаз, Криксиван, Новир, Аптивус и др. Они блокируют фермент, благодаря которому появляются белки вирусных частиц. Ингибирование активности протеазы не дают вирусу заражать здоровые клетки.
Нуклеозидные Зиаген, Видекс, Эпивир, Комбивир, Тризивир воздействуют на ревертазу, или обратную транскрипатзу, которая активирует синтез ДНК, комплементарной вирусной РНК. Таким образом, она незаменима для жизненного цикла фиркса иммунодефицита человека. К ненуклеозидным средствам, воздействующим на ревертазу, относятся: Рескриптор, Вирамун, Стокрин, Интеленс, Эдюрант.
Ингибиторы проникновения, например, Энфувиртид, не дают вирусу проникать в лимфоциты.
Принимать несколько видов таблеток по предписанию врача нужно пожизненно. Кроме того, пациенту требуются медикаменты против развивающихся на фоне ВИЧ заболеваний. Лечиться следует только под наблюдением профессионала. Важными составляющими являются контроль за состоянием здоровья пациента и соблюдение режима принятия медикаментов.
К применяемым лекарственным средствам может развиться сопротивляемость, поэтому есть потребность их частой замены. К минусам терапии можно отнести большое количество побочных эффектов (тошнота, потливость, бессонница, головокружение) и необходимость всю жизнь принимать большое количество медикаментов. Эксперты считают, что в перспективе возможно полное излечение от болезни. Новые средства сейчас находятся в стадии разработки или только испытываются. (PRO140, Ибализумаб). Разрабатываются новые формулы уже известных препаратов, таких как Виаред.PRO 140 препятствует проникновению ВИЧ в клетки и может стать принципиально новым способом. Ибализумаб — это ингибитор проникновения, который показал хорошие результаты при испытании на пациентах с невосприимчивостью к другим ингибиторам.
В декабре 2017 года стало известно, что вирус MG1 нападает на поражённые ВИЧ клетки и сокращает их число. В будущем возможно создание лекарства на его основе.
Какие препараты для лечения ВИЧ-инфекции показали свою эффективность
Лекарства не могут полностью нейтрализовать вирус, но блокируют функцию его основных ферментов и подавляют активность ВИЧ. Таким образом, иммунные клетки организма восстанавливаются. Благодаря приему лекарств от СПИДА и ВИЧ под наблюдением специалиста вирусная нагрузка существенно снижается. Если же этого не происходит, врач разработает новую схему и заменит часть лекарств на другие.
Если у человека наблюдаются симптомы ВИЧ и снижено количество CD4-лимфоцитов, надо проконсультироваться с доктором и купить препараты для лечения ВИЧ-инфекции. Некоторыми из них государство обеспечивает больных бесплатно.
В основном при комбинированной терапии требуется принимать три препарата, подобранные в соответствии с индивидуальными особенностями организма человека. Сложно сказать, какие из них обладают наилучшим действием: это зависит и от стадии, времени начала лечения, состояния пациента и других факторов.
Широко известные, проверенные лекарства, это: Зидовудин, который используется для антиретровирусной терапии с 1987. Ритонавир, один из первых ингибиторов протеазы, появился в 1995-1996 году. С тех пор значительно снизилась смертность больных СПИДом. Невирапин и Нелфинавир используются с 1996 года.
Клинические исследования продолжаются, появляются новые препараты, поэтому есть надежда на то, что лекарство, полностью «убивающее» вирус, будет найдено.
Кроме употребления назначенных лекарственных средств, ВИЧ-инфицированные также принимают витамины и минералы. Эти вещества нужны всем, а у людей с таким заболеванием дефицит витаминов А, Е, B6, B12. Исследования, проведенные в Таиланде и ЮАР, показали, что прием витаминных комплексов способствует торможению развития болезни. Люди с иммунодефицитом имеют высокие риски переломов костей и остеопороза. Согласно исследованиям, проведенным в Южной Каролине, США, витамин D снижает этот риск и укрепляет костную ткань.
Нельзя однозначно сказать, что любые БАДы полезны. Принимать такие добавки лучше по рекомендации врача. Альтернативой также может быть улучшение качества питания, насыщенного питательными веществами. Нельзя считать, что прием таких добавок безусловно полезен для организма. В излишке биологически активные добавки могут даже привести к побочным эффектам. Но при сниженном уровне витаминов добавки положительно влияют на организм и дают ему возможность лучше справиться с вирусом, повышая иммунитет.
К стимуляторам иммунной системы относится Ферран, аналог гемоглобина крови. Его прописывают при иммунодефицитах, так как он повышает сопротивляемость, усиливает иммунитет, мобилизует силы и улучшает восприимчивость к лекарственным препаратам.
Преимущества Феррана:
- улучшение состава крови
- вывод вредных веществ
- подавление инфекций
- доставка медикаментов до поражённых участков
- отсутствие нежелательных побочных действий
Как дополнительное средство усиления резистентности этот препарат незаменим. Его безопасность доказана медицинскими исследованиями и наличием необходимых сертификатов.
xn--80ajzkav.xn--p1ai
Препараты для лечения ВИЧ-инфекции
Лекарственные средства для лечения СПИДа
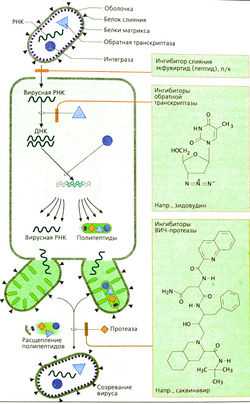 А. Средства для лечения СПИДа
А. Средства для лечения СПИДаРазмножение вируса иммунодефицита человека (ВИЧ), возбудителя СПИДа, можно приостановить только очень активным и целенаправленным лечением, воздействуя на обменные процессы вируса в инфицированной клетке (А). Сначала нуклеокапсид вируса через гликопротеины связывается с СС)4-молекулой Т-хелпера. Затем в дело вступает капсидный белок, который начинает процесс слияния капсида с клеточной мембраной. В инфицированной клетке вирусная РНК должна прежде всего транслироваться в ДНК; это происходит также с помощью вирусного фермента обратной траскриптазы. Двухцепочечная ДНК с помощью вирусного фермента интегразы встраивается в геном клетки-мишени. Далее происходит репликация вируса. ДНК вируса управляет синтезом вирусных РНК и белков (обратной транскриптазы и интегразы, а также структурных белков, находящихся на внутренней стороне вирусной оболочки). Продуктами белкового синтеза являются полипептиды — белки-предшественники, несущие на N-конце жирную кислоту (миристи-новую кислоту), с помощью которой они прикрепляются к внутренней стороне плазмалеммы клетки-мишени. Затем вирусная частица отделяется («отпочковывается») от клетки. Во время этого процесса полипептид, содержащий протеазу, расщепляется на отдельные белки с определенными функциями.
I. Нуклеозидные ингибиторы обратной транскриптазы
К ним относятся зидовудин, ставудин, зальцитабин, диданозин и ламивудин. Эти вещества представляют собой нуклео-зиды с аномальным сахарным остатком, который затем фосфорилируется (см. зидовудин на рис. А). Аномальные трифосфаты блокируют обратную транскриптазу и могут вызывать обрыв синтеза цепи вирусной ДНК. Препараты вводятся перорально. Они различаются по побочным эффектам (например, лейкопения при приеме зидовудина, периферийная нейропатия или панкреатит при приеме других средств) и механизму развития резистентности. Для лечения СПИДа применяют комбинацию из двух препаратов этой группы и одного ненук-леозидного ингибитора, либо одного-двух ингибиторов ВИЧ-протеазы (см. ниже).
Ненуклеозидные ингибиторы
Невирапин и эфавиренц являются активными ингибиторами обратной транскриптазы, т. е. они не нуждаются в фосфорилировании. Побочный эффект —- экзантема и взаимодействие изофермента цитохрома Р450 (CYP) с лекарством.
II. Ингибиторы ВИЧ-протеаз
Препараты препятствуют расщеплению неактивного белка-предшественника и, следовательно, созреванию вируса. Применяются перорально.
Саквинавир можно назвать аномальным пептидом. Его биодоступность ограничена. Другие ингибиторы протеаз: ритонавир, индинавир, нелфинавир, ампренавир. Они характеризуются высокой биодоступностью; ингибируют активность CYP, так что необходимо учитывать возможные взаимодействия с лекарствами. При длительном применении возможно перераспределение жировой ткани в организме и нарушение обмена веществ (гиперлипидемия, инсулиновая резистентность, гипергликемия).
III. Ингибитор слияния
Энфувиртид является пептидом, препятствующим необходимому пространственному изменению белка слияния посредством специфического связывания с ним.
Является резервным терапевтическим средством.
Антиретровирусные средства
Пандемия ВИЧ-инфекции, захватившая сегодня почти все страны, бросает вызов всему медицинскому сообществу. ВИЧ-инфекция развивается постепенно и характеризуется интенсивным размножением вируса, снижением числа лимфоцитов CD4 и тяжелым иммунодефицитом. В силу особенностей обратной транскриптазы ВИЧ (высокая частота ошибок при транскрипции) этот вирус быстро эволюционирует и легко приобретает устойчивость к антиретровирусным препаратам. Благодаря успехам в изучении патогенеза ВИЧ-инфекции и генетических основ устойчивости ВИЧ в короткие сроки был разработан целый ряд препаратов, действующих на обратную транскриптазу или протеазу этого вируса. Найдены различные комбинации препаратов, которые активно подавляют репродукцию вируса, повышают число лимфоцитов CD4 и существенно снижают риск осложнений и смертность от ВИЧ-инфекции. И все же многим больным помочь не удается — из-за устойчивости ВИЧ, побочных эффектов при длительной антиретровирусной терапии и сложности схем лечения. Кроме того, в развивающихся странах, где ВИЧ-инфекция распространена особенно широко, современные препараты, как правило, недоступны. В настоящей главе рассмотрены общие принципы патогенетической терапии ВИЧ-инфекции и описаны отдельные антиретровирусные препараты.
Общие сведения о ВИЧ-инфекции
Главная особенность ВИЧ-инфекции — снижение числа лимфоцитов CD4, ведущее к недостаточности клеточного иммунитета. За 20 лет, прошедших с появления первых сообщений о СПИДе (Gottlieb et al., 1981; Masur et al., 1981), в роли возбудителя почти повсеместно выступал ВИЧ-1. Только в Западной Африке преобладает другой ретровирус — ВИЧ-2. Зрелые вирусы содержат две молекулы одноцепочечной РНК, окруженные нуклеокапсидом и внешней липидной оболочкой. Как и у всех ретровирусов, в геноме ВИЧ имеется три главных гена — gag, pol и env. Хотя гомология аминокислотных последовательностей ВИЧ-1 и ВИЧ-2 составляет около 50%, антиретровирусные препараты могут действовать на них по-разному. Так, на ВИЧ-2 не действует ни один из не-нуклеозидных ингибиторов обратной транскриптазы.
Успехи в изучении патогенеза ВИЧ способствовали более рациональному подходу к разработке новых препаратов и надежных методов лечения и, таким образом, к снижению частоты осложнений и смертности от СПИДа (Palellaetal., 1998). Методы лечения ВИЧ-инфекции быстро развиваются. В то же время неправильное лечение может привести к непоправимым последствиям. Поэтому в США к лечению ВИЧ-инфицированных допускают лишь врачей, прошедших специализацию и имеющих соответствующий опыт (HIV/AIDS Treatment Information Service, 2000).
Патогенез ВИЧ-инфекции
Больные СПИДом особенно восприимчивы к инфекциям и злокачественным новообразованиям. В самом начале пандемии ВИЧ-инфекции ошибочно полагали, что вирус в течение длительного времени пребывает в латентном состоянии и не размножается, и только когда его репродукция возобновляется, болезнь начинает прогрессировать. Однако чувствительные методы выделения вируса в культуре клеток и определения его нуклеиновых кислот показали, что почти для всех нелеченных больных характерна постоянная виремия (Но et al., 1989).
В крупных исследованиях установлены главные прогностические признаки ВИЧ-инфекции: концентрация вирусной (ВИЧ-1) РНК (Mellorset al., 1996) и число лимфоцитов CD4 (Mellors et al., 1997) в крови больного. Это позволило целенаправленно искать способы сдерживать репродукцию ВИЧ в течение длительного времени.
С появлением высокоэффективных антиретровирусных препаратов появилась возможность исследовать патогенез ВИЧ-инфекции. Эти препараты нарушают репродукцию вирусов, снижая концентрацию вирусной РНК в плазме. У ранее нелеченных больных за неделю лечения мощными ингибиторами обратной транскриптазы или протеазы ВИЧ сывороточная концентрация РНК ВИЧ-1 снижается в 10—100 раз. Математическая обработка этих данных показала, что репродукция ВИЧ происходит очень быстро и за сутки образуется около 109 новых вирусов (Но et al., 1995; Perelson et al., 1996; Wei et al., 1995).
Почти 99% вирусов, находящихся в плазме, попадают туда из недавно инфицированных лимфоцитов CD4, средняя продолжительность жизни которых составляет 2,2 сут (Perelson et al., 1997). Предполагают, что есть еще один источник вирусов (по-видимому, это макрофаги), который сохраняется в крови 2 нед (Perelson et al., 1996, 1997). Согласно расчетам, при условии полного подавления репродукции ВИЧ и отсутствия других источников поступления вирусов в кровь за 2—3 года исчезли бы все зараженные клетки и некоторые больные полностью выздоровели бы.
К сожалению, часть покоящихся лимфоцитов CD4 несет вирусы, способные к размножению (Chun et al., 1997; Chun et al., 1998; Finzi et al., 1997). Хотя таких клеток в организме относительно немного, они могут сохраняться несколько месяцев и даже лет. При этом (согласно аналогичным расчетам) для полного излечения ВИЧ-инфекции потребовалось бы подавить репродукцию вируса более чем на 100 лет. Действительно, при отмене антиретровирусных препаратов, даже если вирусная РНК не обнаруживалась уже несколько лет, виремия неминуемо возникает вновь (Davey etal., 1999).
Жизненный цикл ВИЧ
ВИЧ — это РНК-содержащий ретровирус, который размножается в лимфоцитах CD4, макрофагах и дендритных клетках. На схеме жизненного цикла показаны многочисленные мишени, на которые можно воздействовать теми или иными препаратами, чтобы подавить репродукцию вируса. Из них в настоящее время применяются лишь ингибиторы обратной транскриптазы и протеазы ВИЧ, но разрабатываются и новые средства, действующие на другие мишени.
Жизненный цикл ВИЧ начинается с прикрепления к мембране клетки-хозяина, при этом внешняя оболочка вируса сливается с клеточной мембраной. Вирус проникает в клетку за счет связывания гликопротеидов его внешней оболочки (gp41 и gpl20) с клеточными рецепторами (CD4 и рецепторами хемокинов, в частности CCR5 и CXCR4) (Не et а!., 1997; Sodroski 1999). Обычно ВИЧ поражает лишь клетки, несущие и рецепторы CD4, и рецепторы хемокинов. На внешней оболочке вируса находятся трехмерные структуры, напоминающие шипы. Каж. дый такой шип состоит из трех поверхностных гликопротеидов gp 120 и трех трансмембранных гликопротеидов gp41. До контакта вирусного гликопротеида gpI20 с рецептором N-концевой участок (N36) gp41 имеет вид a-спирали. На внешней ее стороне есть гидрофобная щель. В момент контакта gpl20 с рецептором С-концевой участок gp4I (С34) заполняет эту гидрофобную щель, и в результате образуется вытянутая спиральная структура из 6 звеньев — так называемый белок слияния (Sodroski, 1999). При взаимодействии этого белка с клеточной мембраной она сливается с внешней оболочкой вируса, и вирусная РНК оказывается в цитоплазме. На этот этап репродукции ВИЧ действует по крайней мере один из антиретровирусных препаратов (Т-20), проходящих сейчас клинические испытания.
В цитоплазме вирус высвобождает РНК, которая служит матрицей для синтеза комплементарной ДНК. Этот синтез, характерный только для ретровирусов, носит название обратной транскрипции и происходит при участии вирусной обратной транскриптазы. На этот фермент действуют нуклеозидные и ненуклеозидные ингибиторы обратной транскриптазы. Образовавшаяся при обратной транскрипции двухцепочечная ДНК провируса замыкается в кольцо и переходит в ядро. Здесь она под действием второго ключевого фермента ВИЧ — интегразы — встраивается в геном клетки-хозяина. Интеграза также привлекает внимание как возможная мишень антиретровирусных препаратов, но из-за сложного взаимодействия клеточной ДНК. и ДНК провируса при интеграции такие препараты пока не разработаны. Рисунок 51.1. Жизненный цикл ретровирусов на примере ВИЧ-1.Встроившись в геном клетки, ДНК провируса транскрибируется вместе с клеточной ДНК, при этом образуется и клеточная, и вирусная РНК. В дальнейшем вирусная РНК используется для синтеза вирусных белков (в том числе Gag-Pol и Env) или включается в новые вирусы при сборке. Два следующих этапа жизненного цикла ВИЧ — созревание и отпочковывание от клеточной мембраны. В процессе созревания полипротеин Gag-Pol расщепляется протеазой — третьим ключевым ферментом ВИЧ. Зрелые вирусы способны заражать новые клетки. В присутствии ингибиторов протеазы ВИЧ образуются неполноценные вирусы с измененным нуклеокапсидом — заражать клетки они не могут.
Общие принципы антиретровирусной терапии
Эффективность антиретровирусных препаратов определяется тем, насколько снижается и как долго остается низкой концентрация вирусной РНК в плазме (Marschneret al., 1998; O’Brien et al., 1996). Основной принцип лечения состоит в том, чтобы полностью и как можно на более длительный срок подавить репродукцию вируса при наименьших побочных эффектах. Для этого лучше всего подходит комбинированная терапия (HIV/AIDS Treatment Information Service, 2000). Многие больные с трудом привыкают к сложным схемам лечения, и именно несоблюдение схемы лечения — самая частая причина неэффективности лечения и гибели больных. В одном из исследований больным назначали ингибиторы протеазы ВИЧ (индинавир, нелфинавир, саквинавир с ритонавиром) и нуклеозидные ингибиторы обратной транскриптазы — лечение оказалось эффективно, если испытуемые придерживались схемы хотя бы на 95% (Paterson et al., 2000).
Лекарственная устойчивость
При транскрипции РНК с участием обратной транскриптазы ВИЧ возникает множество ошибок. Дело в том, что обратная транскриптаза (как и все полимеразы, использующие РНК в качестве матрицы) лишена З’-экзонуклеазной активности, которая необходима для исправления ошибок. Частота ошибок в каждом цикле репродукции составляет 3,4-10“5 на пару нуклеотидов. Учитывая длину генома ВИЧ (104 пар нуклеотидов), в отсутствие лечения каждая пара нуклеотидов должна ежедневно претерпевать целый ряд мутаций, а каждые 100 сут в геноме вируса должны возникать две точечные мутации одновременно (Coffin, 1995; Wain-Hobson, 1993). Это последнее утверждение предполагает, что точечные мутации не снижают эффективность репродукции, что, по-видимому, неверно.
Неполное подавление репродукции ВИЧ неизбежно приводит к появлению устойчивых штаммов (Havlir and Richman, 1996; Molla et al., 1996). Хотя ненуклеозидные ингибиторы обратной транскриптазы очень эффективны, для развития устойчивости ВИЧ достаточно уже одной точечной мутации в кодоне 103 гена, кодирующего этот фермент. Так как штаммы с такой мутацией есть почти у всех ВИЧ-инфицированных еще до начала лечения, то монотерапия ненуклеозидными ингибиторами обратной транскриптазы бесполезна: сначала концентрация вирусной РНК в плазме снижается (за счет подавления чувствительных штаммов), но уже через несколько недель возрастает вновь (за счет репродукции устойчивого штамма). Напротив, в сочетании с препаратами других групп ненуклеозидные ингибиторы обратной транскриптазы подавляют ВИЧ в течение длительного времени (Staszewski et al., 1999). Мутации накапливаются только при репродукции вируса, поэтому полное ее подавление не только предотвращает снижение числа лимфоцитов CD4, но и препятствует развитию устойчивости (Havlir and Richman, 1996).
В начале антиретровирусной терапии у многих больных обнаруживают штаммы ВИЧ, устойчивые сразу ко многим препаратам. Поэтому, назначая антиретровирусные средства впервые или меняя схему лечения, врач всегда должен учитывать эту возможность и заранее обдумать другие методы лечения, к которым можно будет обратиться при появлении устойчивости (HIV/AIDS Treatment Information Service, 2000).
Для выбора оптимальной схемы лечения важно выявить уже имеющиеся мутации ВИЧ, от которых зависит устойчивость к тому или иному препарату (Durant et al.,1999). Нужно также учитывать, какие схемы лечения применялись ранее и как изменялась концентрация вирусной РНК на фоне каждой из этих схем; сопутствующие заболевания; возможность соблюдения больным сложных схем лечения и его собственные предпочтения. При смене препарата устойчивые штаммы постепенно исчезают из плазмы (уступая место чувствительным), тем не менее они могут неограниченное время сохраняться в тканях (Hirsch et al., 2000; Romanelli and Pomeroy, 2000).
В такой ситуации определение чувствительности к препарату может дать ложноположительный результат. Кроме того, применяемые сейчас методы определения устойчивости надежны только в том случае, если доля устойчивых штаммов в организме достаточно велика. Методы определения устойчивости изучаются в клинических испытаниях.
Когда начинать лечение?
Решение о необходимости антиретровирусной терапии следует принимать индивидуально с учетом как концентрации РНК ВИЧ-1 в плазме, так и числа лимфоцитов CD4. Считается, что лечение следует начинать, если концентрация РНК ВИЧ-1 в плазме превышает 20 000 мл»1 (ее определяют методом полимеразной цепной реакции с обратной транскрипцией) или число лимфоцитов CD4 менее 350 мкл-1. Во всех других случаях имеет смысл отложить начало лечения, так как у больных с меньшей концентрацией вирусной РНК в плазме и большим числом лимфоцитов CD4 кратковременный прогноз весьма благоприятен (Harrington and Carpenter, 2000; Mel-lors et al., 1996; HIV/AIDS Treatment Information Service,2000).
Оценка эффективности лечения
Для оценки эффективности лечения периодически измеряют концентрацию вирусной РНК в плазме (Marsch-ner et al., 1998). В силу индивидуальных генетических особенностей концентрация вирусной РНК может меняться, поэтому до начала лечения ее определяют в двух пробах крови, полученных в разные дни. Важно, чтобы больной в полной мере осознавал необходимость длительное время соблюдать схему лечения, поскольку невыполнение предписаний приводит к устойчивости вируса и ограничивает возможности лечения. В начале лечения концентрацию вирусной РНК определяют каждые 2—4 нед до тех пор, пока она не снизится как минимум в 10 раз, а затем — каждые 3—4 мес (к этому времени она уже не должна обнаруживаться) (HIV/AIDS Treatment Information Service, 2000).
Изредка ВИЧ-инфекция протекает без признаков репродукции вируса и без снижения иммунитета даже в отсутствие лечения. Полагают, что у таких людей клеточный иммунный ответ достаточно силен, чтобы сдержать размножение ВИЧ, и потому заболевание прогрессирует очень медленно. Если это действительно так, то продуманная иммунотерапия могла бы подстегнуть иммунный ответ на вирус у «обычных» ВИЧ-инфицированных и даже позволила бы отказаться от традиционной антиретровирусной терапии. Возможности иммунотерапии ВИЧ-инфекции изучаются сейчас в клинических испытаниях.
Разработка антиретровирусных препаратов
Быстрое развитие антиретровирусной терапии стало возможным благодаря уже существующим программам разработки лекарственных средств, в том числе препаратов для лечения злокачественных новообразований, артериальной гипертонии и вирусных инфекций. У фармацевтических компаний уже был опыт создания и выпуска нуклеозидных ингибиторов обратной транскриптазы с высокой противовирусной и противоопухолевой активностью, а способность ВИЧ размножаться в культуре клеток позволила исследовать такие препараты на эффективность при ВИЧ-инфекции. Была проделана огромная работа по проверке тысяч соединений, и наиболее перспективные из них были модифицированы с целью повысить антиретровирусную активность и биодоступность и свести к минимуму побочные эффекты. Так появился зидовудин. В 1987 г. он стал первым препаратом, разрешенным ФДА для лечения ВИЧ-инфекции. К 2000 г. к применению были допущены еще пять нуклеозидных ингибиторов обратной транскриптазы.
Нуклеозидные ингибиторы обратной транскриптазы до сих пор служат основой антиретровирусной терапии, но поначалу эффективность их была невелика. С помощью этих препаратов удавалось лишь временно приостановить прогрессирование ВИЧ-инфекции и ненадолго отсрочить смерть от СПИДа (Fischl et al., 1987). Поиск более надежных средств с иными механизмами действия привел к открытию ненуклеозидных ингибиторов обратной транскриптазы. Один из первых препаратов этой группы — невирапин — подавлял репродукцию ВИЧ-1 значительно сильнее, чем зидовудин или диданозин (также относящийся к нуклеозидным ингибиторам обратной транскриптазы). Однако энтузиазм по поводу ингибиторов обратной транскриптазы несколько омрачился, когда выяснилось, что в отсутствие строгой схемы лечения этими препаратами быстро возникали устойчивые штаммы ВИЧ.
Одновременно с разработкой ненуклеозидных ингибиторов обратной транскриптазы фармацевтические компании вели поиск препаратов, подавляющих протеазу ВИЧ. В 1985 г. была установлена аминокислотная последовательность этого фермента, в 1986 г. — опубликованы данные о его активности, а в 1989 г. — воссоздана его кристаллическая структура (Navia et al., 1989; Wlodaweret al., 1989). Как и ренин, протеаза ВИЧ относится каспар-татным протеазам. К тому времени уже были синтезированы ингибиторы ренина (негидролизуемые аналоги субстратов или аналоги промежуточных метаболитов) — тот же подход использовали и для создания ингибиторов протеазы ВИЧ (Dreyeret al., 1989). К 1990 г. о разработке ингибиторов этого фермента сообщили сразу несколько лабораторий. В 1992 г. были начаты клинические испытания саквинавира — первого ингибитора протеазы ВИЧ-1, и спустя 3 года он был разрешен ФДА для лечения ВИЧ-инфекции.
С тех пор как была описана трехмерная структура протеазы ВИЧ, поиск ингибиторов этого фермента ведется путем анализа структурно-функциональной зависимости, то есть создания соединений, строение которых обеспечивало бы их заданными исследователем свойствами (Freceret al., 1998; Thaisrivongs and Strohbach, 1999). Первые из синтезированных таким методом ингибиторов протеазы ВИЧ обладали высокой липофильностью и низкой растворимостью и потому плохо всасывались, однако со временем этот недостаток был устранен. Клинические испытания показали, что ингибиторы протеазы ВИЧ хорошо подавляют репродукцию вируса, а устойчивость к ним развивается не так быстро, как к не-нуклеозидным ингибиторам обратной транскриптазы.
Оценка эффективности препаратов в клинических испытаниях
Об эффективности первых антиретровирусных препаратов, как правило, в виде монотерапии, судили по их способности отдалять смертельный исход или развитие оппортунистических инфекций. Впоследствии выяснилось, что предсказать дальнейшее течение ВИЧ-инфекции и оценить эффективность лечения можно по динамике числа лимфоцитов CD4 и концентрации вирусной РНК в плазме. Лучшим стали считать препарат, который сильнее всего снижал концентрацию вирусной РНК.
От длительной монотерапии пришлось отказаться, когда выяснилось, что она способствует развитию устойчивости. Теперь новые препараты испытывают в комбинациях. Однако многие комбинации полностью подавляют репродукцию вируса, и оценить вклад испытуемого препарата не всегда возможно. Кроме того, комбинированная терапия успешно предотвращает оппортунистические инфекции, которые прежде служили важным критерием эффективности. Сейчас эффективность антиретровирусных препаратов в 3-й фазе клинических испытаний оценивают по доле больных, у которых вирусная РНК не определяется на 24-й и 48-й неделях лечения. Схемы лечения различаются количеством таблеток, частотой их приема, требованиями к режиму питания и составу пищи. Различия в эффективности, выявленные в сравнительных испытаниях, зависят скорее от сложности схем, чем от самих препаратов.
В рамках данной главы невозможно осветить результаты клинических испытаний всех антиретровирусных средств. Исследования в этом направлении идут очень интенсивно. Здесь мы приведем лишь некоторые из важнейших испытаний; подробнее см., например, в обзоре Tavel et al. (1999).
Препараты для лечения ВИЧ-инфекции
Нуклеозидные ингибиторы обратной транскриптазы
Обратная транскриптаза синтезирует ДНК провируса на матрице РНК; после этого ДНК провируса встраивается в геном клетки-хозяина. На этом раннем и очень важном для вируса этапе жизненного цикла и действуют ингибиторы обратной транскриптазы. Следовательно, они лишь предотвращают заражение ВИЧ новых клеток, но почти не влияют на уже инфицированные клетки. Все препараты этой группы выступают в роли субстратов для обратной транскриптазы. В цитоплазме они фосфорилируются под действием клеточных ферментов и встраиваются в растущую цепь ДНК. Поскольку у нуклеозидных ингибиторов обратной транскриптазы отсутствует гидроксильная группа в З’-положении рибозного кольца, дальнейший рост ДНК становится невозможным.
Таблица 51.1. Антиретровирусные препараты, разрешенные для применения в США
Международное название | Синонимы | Относительная противовирусная активность |
Нуклеозидные ингибиторы обратной транскриптазы | ||
Абакавир* | 1592U89 | +++ |
Диданозин | ddl; дидезоксиинозин | ++ |
Зальцитабин | ddC; дидезоксицитидин | + |
Зидовудин*-6 | AZT; азидотимидин | ++ |
Ламивудин*’6 | ЗТС | ++ |
Ставудин | D4T | ++ |
Ненуклеозидные ингибиторы обратной транскриптазы | ||
Делавирдин | +++ | |
Ифавиренц | DMP266 | +++ |
Невирапин | B1-RG-587 | +++ |
Ингибиторы протеазы ВИЧ | ||
Ампренавир | VX-478; 141W94 | +++ |
Индинавир | L-735524 (L-524) | +++ |
Лопинавир/ ритонавир* | АВТ-378/г | +++ |
Нелфинавир | +++ | |
Ритонавир | АВТ-538 | +++ |
Саквинавир | ||
в твердых желатиновых капсулах | ++ | |
в мягких желатиновых капсулах | +++ | |
На сегодняшний день ФДА разрешены к применению шесть нуклеозидных ингибиторов обратной транскриптазы (табл .51.1), отличающиеся друг от друга механизма-ми фосфорилирования и побочными эффектами. Их химические формулы приведены на рис. 51.2. Среди этих препаратов есть как проверенные временем (например, зидовудин и диданозин), так и одобренные ФДА сравнительно недавно (абакавир). Нуклеозидные ингибиторы обратной транскриптазы пробовали применять в виде монотерапии или в комбинациях из двух препаратов, но сейчас они входят в состав надежных схем лечения, включающих 3—4 препарата. Недавние исследования показали, что нуклеозидные ингибиторы обратной транскриптазы могут вызвать лактацидоз, выраженную гепатомегалию и жировую дистрофию печени. Фармакокинетические свойства этих препаратов описаны в табл. 51.2.
Зидовудин
Строение и противовирусная активность. Зидовудин (З’-азидо-З’-дезокситимидин) — это синтетический аналог тимидина, действующий на ВИЧ-1, ВИЧ-2 и T-лимфотропные вирусы человека типов 1 и 2 (McLeod and Hammer, 1992). In vitro концентрация зидовудина, на 90% подавляющая репродукцию штаммов ВИЧ-1 (лабораторных и выделенных от больных), составляет 0,03—0,3 мкг/мл. Активность зидовудина в культурах лимфобластов и моноцитов, в которых ДНК провируса еще не встроилась в геном, была гораздо выше, чем в клетках, в которых интеграция уже произошла (Geleziunas et al., 1993). Механизм действия и устойчивость. В клетке зидовудин последовательно фосфорилируется тимидинкиназой до монофосфата, а затем тимидилаткиназой — до дифосфата. Далее под Действием нуклеозиддифосфаткиназы дифосфат превращается в активный зидовудинтрифосфат (Furman et al., 1986). Зидовудин-монофосфат может накапливаться в клетках в высоких концентрациях. Т1/2 зидовудинтрифосфата внутри клетки составляет около 3 ч. конкурируя с дезокси-ТТФ, зидовудинтрифосфат встраивается в растущую ДНК и останавливает ее репликацию. Кроме того, он несколько подавляет активность клеточной ДНК-полимеразы а и митохондриальной ДНК-полимеразы (ДНК-полимеразы у). Зидовудинмонофосфат конкурентно ингибирует клеточную тимидилаткиназу, снижая тем самым уровень дезокси-ТМФ (Furman et al., 1986). С влиянием на ДНК-по-лимеразы и тимидилаткиназу, по-видимому, связаны цитотоксичность и другие побочные эффекты зидовудина.0 0 481
sportguardian.ru
Инъекционный препарат для лечения ВИЧ-инфекции будет готов к 2017 году
На прошлой неделе компания CytoDyn Inc. заявила о том, что результаты продолжающегося расширенного исследования монотерапии препаратом PRO 140 свидетельствуют о «полном подавлении вирусной нагрузки» продолжительностью более одного года, достигая у некоторых пациентов 17 месяцев. В исследование I фазы были включены 23 пациента.
«Компания считает, что, в отличие от широко используемой комбинированной высокоактивной антиретровирусной терапии (ВАРТ), полное подавление вирусной нагрузки с помощью одного препарата PRO 140, безопасного и эффективного антитела, может стать важным методом лечения ВИЧ-инфекции. Компания планирует представить на рассмотрение Управления по контролю качества продуктов питания и лекарственных препаратов США (FDA) протокол второго исследования III фазы по изучению монотерапии PRO 140. В настоящее время CytoDyn проводит базовое клиническое исследование III фазы, где PRO 140 используется как препарат вспомогательной терапии, коммерческая реализация которого намечена на 2017 год».
22 января компания подала в FDA заявку на регистрацию PRO 140 в качестве принципиально нового лекарственного средства, применяемого для терапии ВИЧ-1, у ранее леченных пациентов с вирусологической неэффективностью..
Механизм действия PRO 140 заключается в том, что он блокирует корецептор ВИЧ CCR5 на T-лимфоцитах, тем самым предотвращает проникновение вируса в клетку. На основании собранных к настоящему времени сведений компания CytoDyn утверждает, что PRO 140 не оказывает неблагоприятного действия на опосредованные CCR5 функции иммунной системы.
Согласно данным, изложенным в пресс-релизе, «…результаты недавно проведенного клинического исследования IIb фазы продемонстрировали, что PRO 140 может препятствовать формированию устойчивости вируса у пациентов, временно прекративших прием традиционной лекарственной терапии на несколько недель».
«Известно, что стандартом лечения ВИЧ-инфекции является комбинация антиретровирусных (АРВ) препаратов разных классов, которые нарушают те или иные этапы жизненного цикла вируса. Однако в настоящее время длительно болеющие пациенты сталкиваются с проблемой лекарственной резистентности и нуждаются в новых вариантах лечения (Pennings 2013 г., Cossarini et al. 2013 г.). Компания считает, что потребность в принципиально новом лекарственном средстве отражает неудовлетворенный спрос на инновационные препараты, необходимые все большему числу пациентов с ВИЧ, которые подвергаются интенсивному и длительному лечению и испытывают недостаток эффективных препаратов в условиях неконтролируемой вирусной нагрузки и количества Т-лимфоцитов CD4+».
Согласно информации, приведенной в пресс-релизе, в одном из исследований пациентов со стабильным течением заболевания переводили с ежедневного применения АРВ- препаратов на монотерапию PRO 140 длительностью до 12 недель. «Тем пациентам, у которых супрессия вируса сохранялась, было позволено продолжать монотерапию препаратом PRO 140 еще 60 недель в ходе расширенного исследования».
«В целом три клинических исследования подтвердили концепцию о том, что монотерапия PRO 140 может снижать вирусную нагрузку у ранее леченных пациентов с ВИЧ-1, — утверждается в пресс-релизе. — Если вирусная нагрузка не выявляется, еженедельное введение PRO 140 позволяет сохранять низкую вирусную нагрузку примерно у 50 % пациентов в течение длительного времени (согласно текущим данным — более одного года). Учитывая предварительные результаты, компания полагает, что данный вариант терапии является решением неудовлетворенной медицинской потребности в препаратах для лечения пациентов, инфицированных ВИЧ-1 с неконтролируемой вирусной нагрузкой, независимо от традиционной АРВ-терапии. Больные, у которых дальнейшее продолжение АРВ-терапии неэффективно, могут получить пользу от лечения препаратом PRO 140».
Президент и исполнительный директор компании CytoDyn доктор Надир Пурассан утверждает: «Результаты нашего исследования монотерапии и его расширенного варианта (наряду с данными, полученными в ходе предыдущих исследований препарата PRO 140 у пациентов с ВИЧ с определяемой и неопределяемой вирусной нагрузкой) демонстрируют, что применение PRO 140 может снижать вирусную нагрузку на величину 1,6 log за три недели. После того как вирусная нагрузка станет неопределяемой, PRO 140 может поддерживать супрессию вируса, о чем свидетельствуют результаты нашего текущего исследования. Получение этих данных ускорит процесс регистрации PRO 140 в качестве терапии для пациентов, у которых нет других альтернатив».
Важно отметить, что эти исследования не являются крупномасштабными. Кроме того, указанные пресс-релизы содержат «заявления о перспективах развития компании». Это означает, что «представленные утверждения и информация отражают намерения, планы, ожидания и убеждения компании CytoDyn и подвержены влиянию рисков, неопределенности и других факторов, многие из которых неподвластны контролю компании CytoDyn. Названные факторы могут стать причиной того, что фактические результаты будут существенно отличаться от приведенных заявлений и информации о перспективах развития компании.
Компания CytoDyn отказывается от какого-либо намерения или обязанности публично корректировать или пересматривать любые заявления или информацию прогностического характера, независимо от появления новых данных, будущих событий или иных происшествий, за исключением случаев, предусмотренных действующим законодательством. Читателям не следует излишне полагаться на данные прогностические утверждения».
spid.center
Лечение ВИЧ-инфекции и СПИД
Автор: врач, научный директор АО «Видаль Рус», Жучкова Т. В., [email protected]
Важное значение при лечении ВИЧ-инфицированных пациентов имеет поддержание здоровья и хорошего самочувствия такими немедикаментозными средствами, как правильное питание, избегание сильных стрессов, здоровый образ жизни, а так же регулярный мониторинг состояния здоровья у врачей-специалистов.
Если вам или вашим близким поставлен диагноз «ВИЧ-инфекция» следует как можно раньше обратиться к квалифицированному специалисту. Необходимо также помнить, что самостоятельно поставить себе диагноз после проведения одного анализа на ВИЧ невозможно (имеется высокий процент ложноположительных и ложноотрицательных результатов).
Принцип лечения
Главной задачей лечения ВИЧ- инфекции является затормозить размножение вируса в организме. Для этого был разработан целый ряд противовирусных лекарственных препаратов и еще многие лекарства находятся на стадии клинических испытаний. ВИЧ является ретровирусом, поэтому подобные препараты получили название антиретровирусные. Эти препараты воздействуют на вирус, находящийся в клетках человека, блокируя действие его ферментов и тем самым не давая вирусу размножаться.
В зависимости от принципа действия противоретровирусные препараты делятся на несколько классов: ингибиторы обратной транскриптазы (ламивудин, зидовудин, абакавир, тенофовир и др.), ингибиторы протеазы (ритонавир, индинавир, ампренавир, нелфинавир и др.), ингибиторы слияния/проникновения (энфувиртид), ингибиторы интегразы и др. Некоторые лекарства включают сразу два или три противовирусных препарата одного или разных классов.
Слово «ингибитор» значит «задерживающий или останавливающий». Вирус не может размножаться при блокировании ферментов, которые обеспечивают этот процесс. Различные препараты подавляют вирус на разных стадиях его жизненного цикла.
Как правило, одновременно применяются сразу несколько антиретровирусных препаратов разных классов. Комбинированная терапия снижает риск развития резистентности.
Антиретровирусная терапия должна применяться только по назначению врача, под наблюдением специалиста и в строгом соответствии с инструкциями. Основу лечения составляет скрупулезное выполнение всех рекомендаций врача, регулярный прием противовирусных препаратов и контроль за состоянием здоровья. Несоблюдение режима приема лекарств может привести к тому, что препараты перестанут действовать, то есть выработается резистентность.
Перед началом лечения расскажите врачу об имеющихся у вас хронических заболеваниях и принимаемых лекарствах (некоторые препараты могут быть не совместимы). Уточните у вашего врача, когда и как следует принимать назначенные лекарства (натощак или с пищей, утром или вечером и т.д.). Обо всех побочных эффектах незамедлительно сообщайте доктору.
Помимо противовирусной терапии в лечении ВИЧ-инфекции и СПИДа уделяют внимание профилактике и лечению осложнений (инфекционные заболевания, неврологические нарушения, изменения показателей крови, новообразования).
Результат лечения
Как мы уже говорили, лекарственные препараты, применяемые для лечения ВИЧ-инфекции не «убивают» вирус, а лишь 6локируют функцию основных ферментов вируса, нарушая процесс размножения ВИЧ и подавляя его активность, что выражается в уменьшении в крови числа вирусных частиц («вирусной нагрузки»). Снижение активности ВИЧ приводит к восстановлению числа иммунных клеток (СD4-лимфоциты). Однако следует понимать, что чем позже начато лечение, тем менее эффективным оно будет. Показаниями к началу противовирусной терапии являются либо наличие клинических симптомов болезни, свидетельствующих о недостаточности иммунной системы, либо снижение числа СD4-лимфоцитов менее 500 клеток в 1 мл. крови.
Контроль лечения
Эффективность лечения контролируется путем определения числа СD4-лимфоцитов («иммунный статус») и количества вируса в крови («вирусная нагрузка»). Спросите вашего врача, как часто следует контролировать вирусную нагрузку и состояние иммунитета. Если терапия эффективна, то число CD4-лимфоцитов спустя 3-6 месяцев от начала лечения существенно увеличится, а «вирусная нагрузка» снизится в 100 и 6олее раз. Если же в процессе лечения отмечается увеличение вирусной нагрузки, снижение числа CD4-лимфоцитов и появление новых симптомов заболевания, то данная схема лечения считается неэффективной. В таком случае врач произведет замену как минимум двух противовирусных препаратов.
ВИЧ-инфекция и беременность
Исследования показали, что при использовании комбинированной антиретровирусной терапии ВИЧ- инфицированной женщины при беременности, риск передачи ВИЧ от матери к ребенку значительно снижается. Однако далеко не все препараты для лечения ВИЧ разрешены к использованию при беременности. Поэтому решение о тактике терапии врач принимает совместно с пациенткой, четко обсуждая возможные риски.
Если вы принимаете антиретровирусные препараты, следует заранее сообщить врачу о планировании беременности. Возможно, потребуется смена лекарственных препаратов.
ВИЧ-инфекция и дети
Диагностика ВИЧ-инфекции
СПИД (ВИЧ-инфекция)
Всемирный день борьбы со СПИДом
ВИЧ/ СПИД: социальные аспекты проблемы
www.vidal.ru
Лечение ВИЧ инфекции (антиретровирусная терапия)
Лечение ВИЧ инфекции – это сложный, многогранный и ответственный процесс, который требует серьезного отношения. Причем успех терапии зависит от стараний не только доктора, но и пациента. Положительного эффекта можно достичь лишь при соблюдении большого количества условий. Их должен знать и четко выполнять и врач, и сам больной.
Российская Федерация – это страна, которая имеет внушительный опыт в плане лечения ВИЧ инфекции. Основу составляет антиретровирусная терапия (АРВТ), благодаря которой ВИЧ инфекция перестала звучать как смертельный приговор. Теперь это заболевание рассматривается, как хроническое. С помощью антиретровирусной терапии вирус устранить из организма невозможно, однако, не исключено, что в обозримом будущем такая возможность появиться.
Прием антиретровирусных аппаратов осуществляется для достижения следующих целей:
Вирусологическая цель. Она направлена на остановку размножения вирусных клеток в организме человека. Об успешном достижении поставленной цели можно судить по вирусной нагрузке в крови. Если она находится на неопределяемом уровне, то вирусологическая цель считается достигнутой.
Иммунологическая цель. Она направлена на повышение иммунного статуса пациента. Когда вирусная нагрузка снижается, а в идеале становится неопределяемой, в крови начинает увеличиваться число CD4 лимфоцитов. Они ответственны за иммунологический ответ организма на любые инфекции. Важно, чтобы пациент понимал, что прием антиретровирусных препаратов не помогает напрямую увеличить число CD4.
Клиническая цель. Она направлена на предотвращение развития заболеваний, которые сопутствуют СПИД. То есть, главное в достижении этой цели – позволить организму бороться с ВИЧ инфекцией и не допустить развития СПИД, а значит и заболеваний, которые могли бы привести к летальному исходу.
Лечение ВИЧ инфекции с помощью приема антиретровирусных препаратов базируется на следующих принципах:
Ранее начало терапии (ее следует начинать при падении CD4 ниже отметки в 350 мкл).
Регулярный прием препаратов.
Приверженность к лечению ВИЧ.
Если врач предлагает пациенту начать прием антиретровирусной терапии, не следует от этого предложения отказываться. Более того, если пациент хочет достичь эффекта от терапии, ему необходимо строго соблюдать все рекомендации лечащего доктора. Только так у человека появляется возможность прожить полноценную и долгую жизнь. При этом качество жизни ВИЧ инфицированного человека практически ничем не будет отличаться от качества жизни здорового человека.
Чтобы не упустить тот момент, с которого необходимо начинать прием антиретровирусной терапии, больной должен регулярно обследоваться в Центре СПИД. Дело в том, что без проведения специальных анализов обнаружить у себя симптомы ВИЧ инфекции практически невозможно. Этот вирус разрушает иммунную систему медленно, но планомерно. Поэтому можно не дождаться каких-либо субъективных симптомов на протяжении многих лет. Между тем, время будет упущено.
На то, что необходимо приступать к лечению ВИЧ инфекции, укажут три фактора:
Количество CD4 клеток, отражающие состояние иммунного статуса больногою
Количество вирусных клеток в крови, отражающие такой показатель, как вирусная нагрузка.
Наличие заболеваний, вызванных ВИЧ инфекцией. Эти заболевания носят название оппортунистических. Если они диагностируются у человека, то терапия начинается независимо от его иммунного статуса или вирусной нагрузки.
Чтобы определить количество вируса в крови, врачи проводят специальные анализы. Они выдают результат в численном количестве копий вируса в одном мл крови. Чем выше уровень CD4, тем сильнее иммунитет у человека. Кроме того, в лабораторных условиях определяют процент содержания лимфоцитов CD4 (CD4%). Тем не менее, при назначении терапии, доктора отталкиваются от абсолютного, а не от относительного количества клеток. То есть от количества клеток в литре крови, а не от процентного их соотношения.
Минздрав Российской Федерации рекомендует начинать антиретровирусную терапию, когда количество CD4 клеток начинает колебаться в диапазоне от 200-350 кл/мм3, а вирусная нагрузка превышает 100000 копий/мл.
Следует учитывать, что уровень CD4 – величина непостоянная. Она зависит от огромного количества факторов, среди которых: прием спиртосодержащих напитков, курение, эмоциональные потрясения, иные инфекционные заболевания, негативные условия внешней среды и пр. Поэтому начинать лечение ВИЧ инфекции опираясь исключительно на один показатель, нецелесообразно. Врач должен отследить динамику уровня CD4 на протяжении нескольких месяцев и соотнести полученные результаты с факторами, которые могли бы повлиять на состояние иммунитета человека.
Риск развития оппортунистических болезней повышается при количестве CD4 менее 300 клеток/мм3, так как иммунная защита ослабевает. У больного могут развиться инфекции, сопряженные с диареей, обезвоживанием, потерей массы тела.
Пневмоцистная пневмония – заболевание, которое наблюдается у большинства ВИЧ инфицированных людей, чьи CD4 ниже порога в 200 кл/мм3. Если этот показатель падает ниже 100 кл/мм3, то риск развития серьезных инфекционных заболеваний становится очень высоким.
Это не означает на 100%, что инфекция обязательно возникнет, но люди с таким количеством CD4 значительно рискуют своим здоровьем. Причем лекарственные препараты, направленные на лечение оппортунистических инфекций зачастую наносят здоровью куда больший вред, чем прием антиретровирусной терапии.
Естественно, что перспектива начала приема антиретровирусной терапии беспокоит пациентов, но следует понимать, что без должного лечения ВИЧ инфекция остается смертельно опасной болезнью. Поэтому начинать лечение ВИЧ инфекции нужно своевременно, чтобы не было слишком поздно. Ведь при количестве CD4 менее 200 кл/мм3, смертельно опасные болезни могут манифестировать в любой момент.
Поэтому регулярные запланированные посещения доктора и четкое следование его инструкциям – это необходимость, обеспечивающая сохранность жизни. Когда врач не назначает лечение ВИЧ инфекции, это не значит, что появляться в Центре СПИД больше не нужно. Важно отслеживать состояние своего иммунитета как минимум, раз в год, а иногда и чаще (раз в 6 месяцев или раз в 3 месяца). Во время визита к доктору, он обязательно проинформирует пациента, когда ему необходимо будет явиться в следующий раз.
Кроме того, люди с ВИЧ инфекцией должны по мере необходимости наблюдаться у иных специалистов (окулист, отоларинголог, невропатолог, гинеколог и пр.), а также проходить иные процедуры (рентгенографию легких, УЗИ, ЭКГ и пр.).
Приверженность человека к лечению ВИЧ
Приверженность человека к лечению ВИЧ – это понятие, которое определяет степень вовлеченности или степень участия пациента в своей терапии. Приверженным считается тот пациент, который стремится получать лечение, проявляет заинтересованность собственным здоровьем, а решение о начале антиретровирусной терапии принимается пациентом на основе знаний, полученных в процессе консультирования грамотным инфекционистом.
Целью приверженности является регулярный прием антиретровирусной терапии и возникновение стойкого лечебного эффекта. Чтобы оценить степень приверженности, можно подсчитать количество принятых препаратов, либо пройденных процедур. В итоге, процент выполненных врачебных назначений и будет указывать на показатель приверженности.
Эффективность лечения ВИЧ инфекции напрямую зависит от приверженности пациента терапии. Чем выше приверженность, тем выше вероятность достижения положительного результата. Уровень приверженности зависит от конкретного заболевания. Так, при лечении гипертонической болезни достаточным уровнем приверженности считается 61%. Такой процент, как правило, бывает достаточным для большинства хронических болезней. Однако ВИЧ инфекция выделяется на их фоне. Для того, чтобы антиретровирусная терапия дала положительный эффект, приверженность лечению должна составлять не менее 90-95%.
Необходимость в столь высоком уровне приверженности объясняется особенностями вируса иммунодефицита, а именно его способностью к мутациям. Каждый пропуск дозы антиретровирусного лекарственного препарата создает для вируса условия, в которых он быстро приспосабливается к получаемой терапии и формирует устойчивые клетки. Некоторые лекарственные препараты перестают действовать при наличии 4-6 мутаций, а некоторые всего лишь при одной мутации. То есть, порой бывает достаточно единичного пропуска дозы, чтобы препарат потерял эффективность для конкретного пациента. Вирус получит возможность размножаться несмотря на проводимую терапию.
Еще одна актуальная проблема – это передача устойчивых к терапии штаммов вируса иммунодефицита от одного человека другому. В итоге у зараженного возникает первичная резистентность, то есть изначально человек инфицируется устойчивым штаммом вируса. К примеру, в странах Европейского Союза таких инфицированных насчитывается уже более 10% от общего числа ВИЧ позитивных людей, и эта цифра постоянно увеличивается.
Чем шире распространяются резистентные штаммы вируса иммунодефицита, тем дороже становится терапия, а значит, выживаемость пациентов падает.
Две основные угрозы низкой приверженности антиретровирусной терапии:
Повышение стоимости препаратов, снижение эффективности получаемого лечения.
Увеличение количества людей, инфицированных устойчивыми штаммами вируса.
Лечение ВИЧ и появление резистентности
Вирус иммунодефицита, с одной стороны, скрывается в тех клетках, куда лекарственным препаратам трудно проникнуть. Там он может жить на протяжении многих лет. В качестве подобных резервуаров выступают латентные CD4 лимфоциты и дендритные фолликулярные клетки лимфоидной ткани.
С другой стороны, вирус постоянно мутирует внутри клетки человека. Этот процесс мутации носит название репликации. В процессе репликации вирус копирует генетическую информацию, которая заключена в определенной последовательности нуклеотидов. Именно эту скопированную информацию он в дальнейшем передает следующему поколению вирусов.
Вирус имеет возможность репликации информации благодаря наличию у него белка под названием обратная транскриптаза. Этот белок у вируса работает с погрешностями, допуская ошибки. То есть при сборке каждого нового вируса будет возникать от 5 до 10 мутаций (с учетом того, что ВИЧ имеет около 9000 нуклеотидных пар). Эти мутации для вируса чаще всего смертельны, так как лишают его возможности дальнейшего копирования. Но в некоторых случаях мутация изменяет вирус настолько, что он становится в состоянии выживать даже при условии влияния на него антиретровирусного препарата. Таким образом следующая партия новых вирусов получает надежную защиту и начинают воспроизводить новые клетки, защищенные от губительного действия принимаемых человеком лекарственных средств. В итоге происходит потеря чувствительности вируса к антиретровирусному лечению.
Если ВИЧ мутирует одновременно к нескольким препаратам, то специалисты указывают на возникновение перекрестной резистентности. Возникновение устойчивых к терапии штаммов существенно осложняет процесс лечения ВИЧ положительных пациентов.
Возникновение резистентности ВИЧ
Человек изначально может быть инфицирован устойчивым к антиретровирусному лечению штаммом ВИЧ. В таком случае речь идет о первичной резистентности. Так, в Северной Америке, такая вероятность по разным данным составляет от 1 до 11%, а в странах Европейского Союза от 9 до 21%. Заражение устойчивыми к терапии штаммами с каждым годом растет. Это объясняется просто, ведь первичная резистентность – это чья-то индуцированная резистентность. Второе понятие означает то, что мутации возникли в теле определенного человека при недостаточной эффективности антиретровирусной терапии на фоне вирусной нагрузки.
Риски развития устойчивости штаммов вируса во много зависят от правильности воздействия препарата на организм пациента и от воздействия организма самого пациента на принимаемый препарат. То есть вероятность развития резистентности зависит от фармакокинетики лекарственного средства и от его фармакодинамики.
Любой антиретровирусный препарат необходимо принимать с заданным интервалом времени для того, чтобы он мог правильно всосаться, попасть в кровоток и накопится в тканях в необходимой концентрации. Оказать воздействие на фармакодинамику и на фармакокинетику могут самые разнообразные факторы, среди которых: возраст больного, его пол, время приема пищи, генетические особенности, прием иных препаратов и пр. Все эти факторы необходимо учитывать при подборе антиретровирусного препарата. Если пациент не соблюдает дозировку, принимает лекарственное средство не в установленное время или вовсе пропускает приемы, то это может привести к резистентности. Поэтому высокая приверженность каждого инфицированного – это залог успешной терапии, а значит профилактика резистентности.
Антиретровирусное лечение ВИЧ должен подбирать только врач, с учетом всех возможных факторов, которые могут повлиять на возникновение резистентности к препаратам у конкретного пациента. По мере необходимости, схема лечения может быть откорректирована.
Профилактика резистентности при лечении ВИЧ
Специалисты выяснили, что если уровень копий вируса в крови менее 50 и нагрузка является неопределяемой, то риск развития резистентности штаммов ВИЧ к антиретровирусному лечению очень мал.
С целью профилактики устойчивости ВИЧ к лекарственным препаратам должны соблюдаться следующие принципы:
Регулярный контроль вирусной нагрузки в крови больного.
Четкое следование врачебным рекомендациям. Отходить от схемы, назначенной доктором, категорически запрещено. Антиретровирусный препарат должен приниматься в определенное время и в установленной дозировке. На уровень его всасывания может оказать влияние диарея, рвота, прием иных лекарственных средств, болезни. Важно, чтобы пациент своевременно оповещал врача об имеющихся у него проблемах.
Впервые начатая антиретровирусная терапия должна быть качественно подобрана. От этого напрямую зависят риски развития резистентности.
Резистентными штаммами ВИЧ можно заразиться повторно. Иногда в организм человека проникают два и более штамма вируса (коинфекция). Так, каждый четвертый инфицированный, проживающий в Сан-Франциско имеет резистентность к одному и более антиретровирусному препарату. Чтобы этого не произошло, необходимо соблюдать меры профилактики передачи ВИЧ.
Получение новых знаний. Человек с ВИЧ инфекцией должен постоянно пополнять свой багаж знаний об имеющемся у него заболевании. Источником информации могут выступать СМИ, лечащий доктор, популярная и научная литература. Чем глубже пациент вникает в суть проблемы, чем больше он имеет знаний относительно сути терапии болезни, тем выше шансы того, что он не допустит ошибок, приводящих к резистентности.
Тем не менее, базовой защитой от резистентности на данный момент времени остается неопределяемая вирусная нагрузка.
Автор статьи: Алексеева Мария Юрьевна, врач-терапевт, специально для сайта ayzdorov.ru
kakbyk.ru
