Что такое рак крови и как его распознать? — Центральная городская больница № 7
О том, как распознать рак крови на ранней стадии и методах его лечения рассказал главный гематолог Екатеринбурга, заведующий отделением гематологии ЦГБ № 7 Вячеслав Семенов.
Вячеслав Андреевич, какие есть симптомы у лейкоза? Может быть, недомогание или еще что-то?
Острый лейкоз это злокачественное опухолевое заболевание из клеток крови. Возникает он в костном мозге из незрелых предшественников лейкоцитов — бластов. В норме количество бластов в костном мозге не превышает 5%, в кровь же они попадать не должны. При развитии острого лейкоза нормальные бласты превращаются в опухолевые и начинают активно размножаться, их процент значительно увеличивается (более 20%), они начинают попадать и в кровь. Таким образом, заподозрить острый лейкоз можно только сдав общий анализ крови, где будут подсчитаны лейкоциты, тромбоциты, эритроциты, гемоглобин и могут быть выявлены бласты.
Какие формы лечения существуют? Это сразу же химиотерапия или может быть и амбулаторное лечение?
В настоящее время лечение острых лейкозов всегда начинается с химиотерапии — это инфузии (капельницы), или таблетки химиопрепаратов. Химиопрепараты достаточно токсичны, но только таким образом они способны уничтожить опухолевые клетки. И, тем не менее, даже они далеко не всегда могут полностью излечить пациента от острого лейкоза. Некоторые виды острых лейкозов требуют дальнейшей пересадки костного мозга (трансплантации), однако, пересадка может быть эффективна только при наступлении ремиссии (исчезновения опухолевых бластов на этапе химиотерапии). Создаются и новые препараты, которые могут воздействовать в большей степени на опухолевые клетки и в меньшей степени на здоровые клетки. Лечение острого лейкоза может быть только в специализированном стационаре, специалистами, имеющими опыт проведения химиотерапии. После наступления выздоровления возможно продолжить поддерживающую терапию, направленную на предотвращение возвращения болезни (рецидива) амбулаторно.
Химиопрепараты достаточно токсичны, но только таким образом они способны уничтожить опухолевые клетки. И, тем не менее, даже они далеко не всегда могут полностью излечить пациента от острого лейкоза. Некоторые виды острых лейкозов требуют дальнейшей пересадки костного мозга (трансплантации), однако, пересадка может быть эффективна только при наступлении ремиссии (исчезновения опухолевых бластов на этапе химиотерапии). Создаются и новые препараты, которые могут воздействовать в большей степени на опухолевые клетки и в меньшей степени на здоровые клетки. Лечение острого лейкоза может быть только в специализированном стационаре, специалистами, имеющими опыт проведения химиотерапии. После наступления выздоровления возможно продолжить поддерживающую терапию, направленную на предотвращение возвращения болезни (рецидива) амбулаторно.
Какие анализы нужно сдавать, чтобы выявить лейкоз на ранней стадии?
Основным и самым простым анализом для выявления острого лейкоза является общий анализ крови. Его необходимо сдавать при любом появившемся ухудшении самочувствия, особенно при наличии признаков инфекции (температура, боли в горле) или кровоточивости. Здоровым людям рекомендую сдавать общий анализ крови раз в полгода.
Его необходимо сдавать при любом появившемся ухудшении самочувствия, особенно при наличии признаков инфекции (температура, боли в горле) или кровоточивости. Здоровым людям рекомендую сдавать общий анализ крови раз в полгода.
- 30 июля 2020 в 15:38
- 39 590
Общий анализ крови
Общий анализ крови — лабораторный анализ, позволяющий определить концентрацию гемоглобина, количество эритроцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC), количество лейкоцитов и тромбоцитов, дополнительно количество ретикулоцитов. А также общий клинический анализ крови не является полным без микроскопии лейкоцитарной формулы и определения неспецифического показателя воспаления — скорости оседания эритроцитов (СОЭ).
Лейкоцитарная формула – это процентное соотношение различных видов лейкоцитов – бластов, промиелоцитов, миелоцитов, метамиелоцитов, палочкоядерных нейтрофилов, сегментоядерных нейтрофилов, эозинофилов, базофилов, моноцитов, лимфоцитов. Кроме этого врач при микроскопии окрашенного мазка крови описывает различные изменения клеток, например, изменения эритроцитов (анизоцитоз, пойкилоцитоз, микроцитоз, макроцитоз, гипохромия, гиперхромия и т.п.). Метод незаменим в диагностике гематологических заболеваний, так как позволяет обнаружить и описать бласты и юные клетки, заподозрить лейкоз.
Кроме этого врач при микроскопии окрашенного мазка крови описывает различные изменения клеток, например, изменения эритроцитов (анизоцитоз, пойкилоцитоз, микроцитоз, макроцитоз, гипохромия, гиперхромия и т.п.). Метод незаменим в диагностике гематологических заболеваний, так как позволяет обнаружить и описать бласты и юные клетки, заподозрить лейкоз.
Бласты, промиелоциты, миелоциты, метамиелоциты в норме в периферической крови не обнаруживаются.
Подсчет лейкоцитарной формулы проводится не только в целях диагностики заболеваний крови, но и для выявления изменений, характерных для инфекционных, воспалительных заболеваний, а также используется для оценки тяжести состояния и эффективности проводимой терапии.
Ретикулоциты – юные формы эритроцитов, которые содержат зернистонитчатую субстанцию, выявляемую при помощи специальной окраски. Ретикулоциты образуются в костном мозге из нормобластов, где дозревают в течение 1 — 2 дней, после чего поступают в периферическую кровь. Время созревания ретикулоцитов до зрелых эритроцитов в периферической крови около 2-х дней. Число ретикулоцитов в крови отражает регенеративные свойства костного мозга и используется для дифференциальной диагностики вида анемии.
Время созревания ретикулоцитов до зрелых эритроцитов в периферической крови около 2-х дней. Число ретикулоцитов в крови отражает регенеративные свойства костного мозга и используется для дифференциальной диагностики вида анемии.
Целесообразно для оценки тяжести анемии использовать «ретикулоцитарный индекс»:
% ретикулоцитов х гематокрит больного / 45 х 1,85
(где: 45 — нормальный гематокрит, а 1,85 — количество суток необходимых для поступления новых ретикулоцитов в периферическую кровь).
- индекс < 2 — свидетельство гипопролиферативного компонента анемии;
- индекс > 2 — 3 — свидетельство увеличения образования эритроцитов.
Скорость оседания эритроцитов (СОЭ) – неспецифический показатель воспаления. При острых воспалительных и инфекционных процессах изменение скорости оседания эритроцитов отмечается через 24 часа после повышения температуры и увеличения числа лейкоцитов.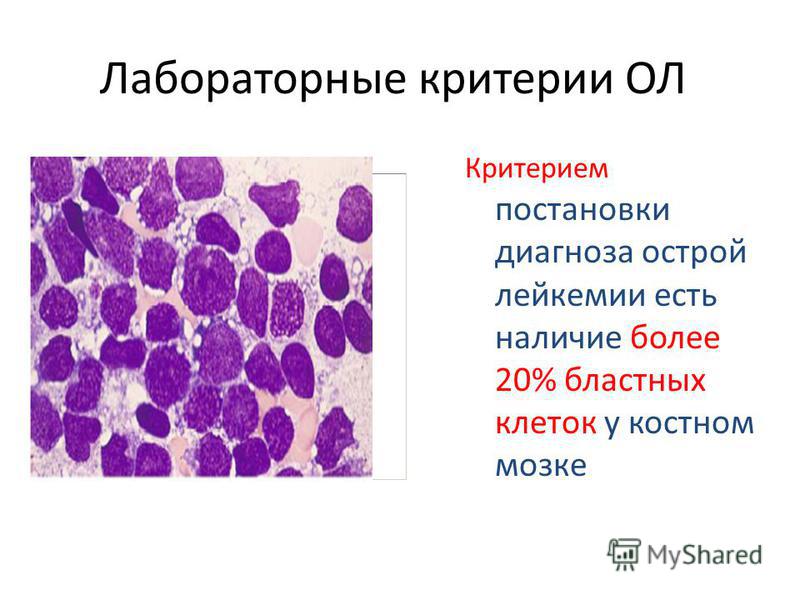 При хроническом воспалении повышение СОЭ обусловлено увеличением концентрации фибриногена и иммуноглобулинов. Определение СОЭ в динамике, в комплексе с другими тестами, используют в контроле эффективности лечения воспалительных и инфекционных заболеваний.
При хроническом воспалении повышение СОЭ обусловлено увеличением концентрации фибриногена и иммуноглобулинов. Определение СОЭ в динамике, в комплексе с другими тестами, используют в контроле эффективности лечения воспалительных и инфекционных заболеваний.
Острый лимфобластный лейкоз (ОЛЛ) у детей и подростков
Три фазы лечения
Лечение ОЛЛ включает в себя 3 фазы и длится от 2 до 3 лет. Основным методом лечения ОЛЛ является химиотерапия. В химиотерапии используются мощные лекарственные препараты для остановки роста опухолевых клеток, уничтожая их или препятствуя их делению. Детям чаще всего назначают комбинацию различных лекарственных препаратов. Эти препараты могут вводиться в кровоток (внутривенно), приниматься внутрь (перорально) или же вводиться непосредственно в спинномозговую жидкость (интратекально).
Выбор метода химиотерапии и лекарственных средств зависит от группы риска ребенка. Дети с лейкозом высокого риска обычно получают больше противоопухолевых препаратов и/или более высокие дозы, чем дети с ОЛЛ низкого риска.
1. Индукция
Целью индукционной терапии является уничтожение бластных клеток в крови и костном мозге и перевод заболевания в ремиссию. Эта фаза обычно длится 4–6 недель. В это же время для уничтожения бластных клеток, остающихся в спинномозговой жидкости, может быть назначена сохраняющая терапия центральной нервной системы (ЦНС) (также называемая профилактической терапией ЦНС). В этом случае препараты вводятся в заполненное жидкостью пространство между тонкими слоями ткани, покрывающими спинной мозг (интратекально).
Для лечения используется комбинация химиотерапевтических препаратов. Эти препараты могут включать в себя винкристин, стероиды и пэгаспаргазу или аспарагиназу Erwinia, иногда с препаратом антрациклинового ряда, таким как доксорубицин или даунорубицин. В некоторых протоколах во время индукционной терапии применяют схему лечения, включающую циклофосфамид, цитарабин и 6-меркаптопурин.
2. Фаза консолидации/интенсификации
 Эта фаза обычно длится 8-16 недель.
Эта фаза обычно длится 8-16 недель.Пациенту назначают различные лекарственные средства, такие как циклофосфамид, цитарабин и или 6-меркаптопурин (6-МП). Также может назначаться метотрексат с терапией под защитой лейковорином или без нее.
3. Фаза стабилизации/продолжения
Целью поддерживающей терапии, последней и наиболее долгой фазы, является уничтожение любых опухолевых клеток, которые могли бы выжить после первых 2 фаз. Фаза стабилизации может продолжаться 2 или 3 года.
Эта фаза может включать в себя применение таких препаратов, как метотрексат, винкристин, стероиды, 6-меркаптопурин (6-МП). Пациентам с высоким риском могут назначаться антрациклиновые препараты, циклофосфамид и цитарабин.
ОЦЕНКА ЭКСПРЕССИИ CD45 ПРИ АНАЛИЗЕ ПОПУЛЯЦИИ БЛАСТНЫХ КЛЕТОК У ДЕТЕЙ С ОСТРЫМИ ЛЕЙКОЗАМИ
Лабораторная диагностика острых лейкозов (ОЛ) начинается с выявления в периферической крови и костном мозгу бластных клеток, которые идентифицируются методом световой микроскопии. Иммунодиагностика, как следующий этап диагностики, основана на сопоставлении морфофункциональных и иммунофенотипических характеристик лейкозных бластов и нормальных/нетрансформированных клеток гемопоэза. Первым шагом иммунофенотипирования является выделение пула злокачественных клеток из общей популяции. Для этого необходимо отделить собственно бластные клетки от детрита, слипшихся клеток, которые могут в разном количестве присутствовать в анализируемом образце, а также от некоторого количества нормальных клеток, которые могут сохраняться в пробе. Надо также помнить о возможном разведении образца периферической кровью. Все эти факторы могут серьезно повлиять на конечный результат исследования. Недостаточно четкое гейтирование (выделение бластной популяции) может привести к неверным выводам при анализе иммунофенотипа.
Иммунодиагностика, как следующий этап диагностики, основана на сопоставлении морфофункциональных и иммунофенотипических характеристик лейкозных бластов и нормальных/нетрансформированных клеток гемопоэза. Первым шагом иммунофенотипирования является выделение пула злокачественных клеток из общей популяции. Для этого необходимо отделить собственно бластные клетки от детрита, слипшихся клеток, которые могут в разном количестве присутствовать в анализируемом образце, а также от некоторого количества нормальных клеток, которые могут сохраняться в пробе. Надо также помнить о возможном разведении образца периферической кровью. Все эти факторы могут серьезно повлиять на конечный результат исследования. Недостаточно четкое гейтирование (выделение бластной популяции) может привести к неверным выводам при анализе иммунофенотипа.
Нашей задачей было проанализировать разли-
чия в экспрессии общелейкоцитарного антигена CD45 на поверхностных мембранах нормальных лимфоцитов и бластов для иммуноцитофлюориметрического разграничения зрелых лимфоцитов и лейкемических клеток при диагностике острых лейкозов.
ОБЪЕКТ И МЕТОДЫ ИССЛЕДОВАНИЯ
В настоящее исследование включены пациенты (n = 74) с ОЛ, находившиеся на лечении в Отделении онкогематологии для детей Института неотложной и восстановительной хирургии им. В.К. Гусака АМН Украины в период 2005–2007 гг. Среди обследованных было 25 девочек (33,8%) и 49 мальчиков (66,2%). Средний возраст пациентов — 7,1 года. Самому младшему ребенку было 3 мес, самому старшему больному — 18 лет. У всех пациентов было проведено иммунофенотипирование методом проточной
цитометрии. Для анализа светорассеяния нормальных лимфоцитов использовали венозную кровь гематологически здоровых доноров (n = 19).
Материалом для проточноцитометрического исследования у больных с ОЛ являлись костный мозг и периферическая кровь. Вид подготовки пробы по протоколу: окрашивание — лизис — отмывка. Процедура настройки прибора и контроль качества его работы осуществлялся сервисной службой украинского представителя Becton Dickinson (BD) фирмой Bioline-Ukraine. Анализ проводили с помощью программного обеспечения FACSComp (BD), программа CellQUEST. При учете результатов регистрировали как процент клеток, экспрессирующих маркер, так и среднюю интенсивность флюоресценции (СИФ), которую выражали в условных единицах (усл. ед.), соответствующих среднему каналу максимального свечения маркера. Позитивность определяли по отношению к негативному изотипическому контролю. Статистическую обработку полученных данных проводили с помощью стандартной прикладной программы Microsoft Ex- cel 2003, рассчитывая средние значения показателей, ошибку средней и достоверность различий по t-критерию Стьюдента. Коэффициент корреляции r рассчитывали по Пирсону.
При учете результатов регистрировали как процент клеток, экспрессирующих маркер, так и среднюю интенсивность флюоресценции (СИФ), которую выражали в условных единицах (усл. ед.), соответствующих среднему каналу максимального свечения маркера. Позитивность определяли по отношению к негативному изотипическому контролю. Статистическую обработку полученных данных проводили с помощью стандартной прикладной программы Microsoft Ex- cel 2003, рассчитывая средние значения показателей, ошибку средней и достоверность различий по t-критерию Стьюдента. Коэффициент корреляции r рассчитывали по Пирсону.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Объектом исследования при диагностике ОЛ являлась популяция лейкемических клеток, которую было необходимо выявить в общей массе клеток и охарактеризовать. Анализ клеточной популяции методом проточной цитометрии основан на измерении отдельных клеток (или какой-либо «биологической частицы», включая изолированное ядро, хромосомные препараты или микробиологические организмы) в жидком потоке, во время их прохождения через монохроматический свет, продуцируемый лазером. Физические свойства, такие как размер и диаметр ядра, наличие цитоплазматических гранул, могут быть измерены у отдельной неокрашенной клетки. На основании указанной ин-
Физические свойства, такие как размер и диаметр ядра, наличие цитоплазматических гранул, могут быть измерены у отдельной неокрашенной клетки. На основании указанной ин-
формации мы можем разделить все лейкоциты на 3 основные популяции: лимфоциты, гранулоциты и моноциты. Анализ клеток при ОЛ в целом соответствует тому, что используется при лимфопролиферативных заболеваниях. Для этого выделяют определенную популяцию клеток и осуществляют более прицельный анализ с помощью логического ограничения (гейтирования) по физическим характеристикам клеток и/или на основании экспрессии определенного маркера.
На двухмерных гистограммах (FSC/SSC), где ось x отражает размеры клеток, а ось y — гранулярность, положение нормальных клеток определяется в зависимости от их физических параметров (рис. 1).
Рис. 1. Расположение кластеров нормальных клеток
Из представленных данных видно, что лимфоциты, как клетки довольно небольшого размера, с невысокой степенью гранулярности, имеют низкие значения как по оси x, так и по оси y. Моноцитарный гейт касается лимфоцитарного гейта с превышением значения SSC в 1,5 раза. Гранулоцитарный гейт касается моноцитарного гейта и распространяется вверх по всей оси SSC.
Моноцитарный гейт касается лимфоцитарного гейта с превышением значения SSC в 1,5 раза. Гранулоцитарный гейт касается моноцитарного гейта и распространяется вверх по всей оси SSC.
Анализ клеток при ОЛ также начинается с выделения популяции бластных клеток. В большинстве случаев он ведется в полигоне, по светорассеянию, соответствующему лимфоцитам. Если количество бластных клеток велико (70–90%), анализируется весь регион. Если популяция малоклеточная (до 50%) и присутствуют в большом количестве оставшиеся нормальные лимфоциты, то по параметрам светорассеяния невозможно разграничить бластные клетки и нормальные лимфоциты периферической крови (ЛПК). Как видно на рис. 2, популяция бластов вследствие большой гетерогенности клеток, входящих в ее состав, не может быть идентифицирована по параметрам FSC/SSC. Поэтому для более детальной характеристики клеточного полигона мы анализировали уровень экспрессии CD45 в сочетании с боковым светорассеянием (SSC/CD45). Оценка экспрессии данного антигена представляется важной потому, что общелейкоцитарный антиген CD45 (трансмембранный гликопротеин) присутствует на всех лейкоцитах вне зависимости от степени дифференцировки, однако уровень экспрессии может быть различным на нормальных и патологически измененных клетках.
В подавляющем большинстве проанализированных нами случаев ОЛ гистограмма SSC/CD45 (ось x отражает уровень экспрессии CD45, а ось y — гранулярность) позволяла более точно, по сравнению с возможностями гистограммы FSC/SSC, разделить низкогранулярные клетки на нормальные (нетрансформированные) лимфоциты и опухолевые (лейкемические) бласты, то есть выявить патологическую популяцию. На рис. 3 показано, что бластные клетки занимают по оси x (на гистограмме справа) место, которое пустует в образце здорового донора. То есть, бластные клетки, обладая одинаковой гранулярностью с нормальными лимфоцитами, имеют более низкий уровень экспрессии CD45.
Однако визуальная оценка интенсивности экспрессии CD45 не позволяет обеспечить абсолютную надежность гейтирования, так как можно отмечать случаи, когда часть или все лейкозные клет-
Рис. 2. Расположение бластной популяции при остром лейкозе
ки отрицательны по этому антигену или значения экспрессии CD45 приближаются к таковым на нор-
мальных лимфоцитах.
Мы проанализировали и такие характеристики антигена CD45, как плотность его распределения на мембране позитивных клеток по СИФ. Зна-
чение показателей интенсивности флюоресценции
в настоящее время активно изучается с точки зре
ния возможности их потенциального использова-
ния для повышения точности диагностики лейкозов, для получения более глубокой информации о биологической сущности бластных клеток, что мо-
жет оказаться полезным для прогнозирования исхода заболевания. При учете результатов мы реги-
стрировали как процент клеток, экспрессирующих маркер CD45, так и СИФ. СИФ во всех пробах с отрицательным изотипическим контролем определялась в диапазоне от 2,9 до 4,5 усл. ед. как по оси FL1 (соответствующей МкАТ, меченным FITC), так и по оси FL2 (соответствующей МкАТ, меченным РЕ). Диапазон СИФ маркерa CD45 на бластных клетках колебался от 25 до 1400 усл. ед., что в 10–50 раз превышало интенсивность свечения изотипического контроля и исключало возможность ошибки.
В результате анализа 19 образцов ЛПК здоровых доноров мы установили, что интенсивность экспрессии CD45 на ЛПК в контрольной группе колебалась от 212 до 576,3 усл. ед. При фенотипировании 74 больных ОЛ (В-ОЛЛ, n = 54; Т-ОЛЛ, n = 14; ОМЛ, n = 6) на этапе диагностики выявлено, что зрелые лимфоциты отличались от бластов более яркой экспрессией CD45 во всех случаях. На одномерной гистограмме были хорошо различимы два пика CD45+-клеток (рис. 4). Пик с более высокой плотностью экспрессии соответствовал оставшимся нормальным клеткам и располагался правее по оси х. СИФ CD45 на остаточных нормальных лимфоцитах колебалась от 235,0 до 506,3 усл. ед., что было близко к таковым показателям ЛПК здоровых доноров.
Рис. 4. Одномерная гистограмма СИФ CD45+-клеток
Эффективность разделения лимфоцитов и бластов при ОЛЛ подтверждена на основании того, что на лимфоцитах отсутствовали маркеры клетокпредшественников (TdT, CD10 и CD34), которые были экспрессированы на бластах различных линий дифференцировки.
Интенсивность экспрессии CD45 на бластах в группе пациентов с ОЛ варьировала от 13,32 до 201,65 усл. ед. Таким образом, экспрессия панлейкоцитарного антигена CD45 на ЛПК здоровых доноров и остаточных нормальных лимфоцитах пациентов с ОЛ была значительнее интенсивной, чем на бластных клетках. На рис. 4 показана одномерная гистограмма СИФ CD45+-клеток (р ≤ 0,001) у пациентов с ОЛ. Правый пик соответствует оставшимся нормальным лимфоцитам, левый — популяции бластов. Цифровые значения полученных результатов отражены в таблице.
Таблица Сопоставление СИФ CD45 лимфоцитов и лейкемических бластов
Нозологические группы | СИФ CD45 (усл. ед.) | |
лимфоциты | бласты | |
Здоровые лица — доноры, n = 19 | 393,65 ± 11,0 | – |
В-ОЛЛ, n = 54 | 203,34 ± 11,2 | 142,7 ± 25,3* |
Т-ОЛЛ, n = 14 | 197,8 ± 24,3 | 99,6 ± 27,7* |
ОМЛ,n = 6 | 221,1 ± 2,7 | 113,6 ± 21,8* |
*p < 0,001.
Рис. 3. Уровень экспрессии CD45 на бластных клетках и нормальных лимфоцитах (слева — здоровый донор, справа — пациент с ОЛ)
Различия СИФ CD45 лимфоцитов и бластов были достоверны во всех группах больных ОЛ, что подтверждает визуальную информацию раздельного расположения кластеров этих типов клеток на гистограммах, учитывающих экспрессию CD45.
Отличия СИФ CD45 лимфоцитов и бластов пациентов с различиными формами ОЛ представлены графически на рис. 5.
Рис. 5. СИФ CD45 на лимфоцитах и бластных клетках при различных формах ОЛ
Таким образом, при выполнении иммунофенотипической диагностики показатель СИФ общелейкоцитарного маркера CD45 помогает отличить сохранившиеся нормальные клетки от бластов и благодаря этому избежать ошибочных заключений при характеристике ОЛ. При анализе лейкозов с наличием бластных клеток с атипичной экспрессией антигенов СИФ CD45 можно рассматривать как дополнительный критерий дифференциальной диагностики цитологических вариантов ОЛ.
ВЫВОДЫ
По параметрам светорассеяния и экспрессии антигена CD45 бластные клетки четко характеризуются невысоким уровнем гранулярности и низким уровнем экспрессии CD45 (СИФ 118,6 ± 13,1) по сравнению с лимфоцитами (СИФ 393,65 ± 11,0). Гейтирование по CD45 позволяет достаточно точно идентифицировать лимфоциты при ОМЛ и цитологических вариантах ОЛЛ, что является удобным средством идентификации лейкемических клеток, обычно занимающих (на гистограмме SSC/CD45) то положение, где располагается малое количество сохранившихся нормальных клеток.
ЛИТЕРАТУРА
Перехрестенко ПМ, Назарчук ЛВ, Федоренко ЗП, Суханова ТГ. Стан захворюваності злоякісними новоутвореннями лімфатичної та кровотворної тканини населення України. Укр журн гематол трансфузіол 2003; (4): 5–10.
Jaffe ES, Harris NL, Stein H, Vardiman JW. Pathology and genetics of tumours of hematopoietic and lymphoid tissues. Lyon: IARC Press, 2001. 352 p.
Бутенко ЗА, Глузман ДФ, Зак КП и др.
 Цитохимия и электронная микроскопия клеток крови и кроветворных органов. Киев: Наук думка, 1974. 248 с.
Цитохимия и электронная микроскопия клеток крови и кроветворных органов. Киев: Наук думка, 1974. 248 с.Бутенко ЗА. Стволовые кроветворные клетки и лейкоз. Киев: Наук думка, 1978. 179 с.
Буглова СЕ, Белевцев МВ, Потапнев МП. Значение интенсивности флюоресценции маркеров дифференцировки в
иммунофенотипической диагностике острых лейкозов у детей. Гематол трансфузиол 2002; 47 (1): 6–9.
Тупицын НН. Иммунодиагностика гемобластозов. В кн: Клиническая онкогематология. Под ред МА Волковой. Москва: Медицина, 2001: 124–45.
Зуева ЕЕ, Афанасьев ББ, Тотлян АА. Иммунофенотипическая характеристика острых лейкозов методом проточной цитометрии. Мед иммунол 2004; 6 (1–2): 9–24.
Сейц ИФ, Луганова ИС. Биохимия клеток крови и костного мозга в норме и при лейкозе. Ленинград: Медицина, 1967. 331 с.
Тупицын НН, Андреева ЛЮ, Кадагидзе ЗГ. Иммунодиагностика гемобластозов человека: пособие для врачей.
 Москва: РОНЦ, 2003. 42 с.
Москва: РОНЦ, 2003. 42 с.Тупицын НН. Лимфоциты и иммунокомпетентная система. В кн: Руководство по гематологии. Под ред АИ Воробьева. Т 1. Москва: Медицина, 2002: 106–25.
Leucocyte typing VII. White cell differentiation antigens. Proc 7th Intern Conf Ed by D Mason et al. Oxford: Univ Press, 2002. 945 p.
Глузман ДФ, Скляренко ЛМ, Надгорная ВА, Крячок ИА. Диагностическая иммуноцитохимия опухолей. Киев: МОРИОН, 2003: 156 с.
Глузман ДФ, Абраменко ИВ, Скляренко ЛМ и др. Диагностика лейкозов. Атлас и практическое руководство. Киев: МОРИОН, 2000. 224 с.
Galigiuri MA, Strout MP, Gilliland DG. Molecular biology of acute myeloid leukemia. Semin Oncol 1997; 24 (1): 32–44.
Bakels V, Van Oostveen JW, Geerts ML,
et al. Diagnostic and prognostic significance of clonal T-cell receptor beta gene rearrangements in lymph nodes of patients with mycosis funqoides. J Pathol 1993; 170: 249–55.Delabesse E, Bernard M, Meyer V,
et al. TAL1 expression does not occur in the majority of T-ALL blasts. Br J Haematol 1998; 102: 440.
TAL1 expression does not occur in the majority of T-ALL blasts. Br J Haematol 1998; 102: 440.Bain B. Leukemia diagnosis. 2nd ed. Oxford etc: Blackwell Science, 1999. 200 p.
Imamura N, Kriatchok IA, Klimenko VI. Expression and point mutation of p53 supressor oncogene in patients with myelodysplastic syndrome among atomic-bomb survivors and Chernobyl accident. Victims Exp Oncol 1996; 18 (2): 333–7.
Дневник обреченной | Статьи | Известия
«Меня зовут Настя Калитенко, я с Украины, из города Одесса. Мой диагноз — «острый лимфобластный лейкоз с поражением ЦНС». Лечусь в Израиле уже пять месяцев с хвостиком, прошла три курса химиотерапии, но ремиссии так и не достигла. В моем случае единственным вариантом лечения остается пересадка костного мозга. Ее стоимость $154 тыс. На лечение до этого момента уже потрачено $100 тыс. Все материальные возможности нашей семьи абсолютно исчерпаны. Пересадка костного мозга нужна срочно, без нее у меня есть максимум два месяца.
И денег на пересадку тоже нет.
До заболевания вела достаточно активный образ жизни. Училась на юриста на третьем курсе. Теперь пришлось перейти на заочную форму обучения. В университете часто организовывала общественные акции помощи детским домам и болеющим детям. Занималась бальными танцами, закончила кандидатом в мастера спорта.
Время от времени я веду дневники.
О моей болезни мы узнали 14 декабря прошлого года. За две недели до этого началась слабость. Я чувствовала себя терпимо, в принципе просто была усталость, и все говорили «ты бледная». Мама, как все мамы в таких случаях, сказала сходить к участковому. Тот выписал направление на анализ крови. На следующее утро я сдала кровь и ждала спокойно результатов. Вечером позвонила женщина, которая брала кровь, и сказала срочно ехать в больницу (была суббота) и не ждать даже понедельника.
Мы, конечно, собрались и поехали. В Одесской областной больнице зашли в детское гематологическое отделение, был дежурный врач. Он спокойно просмотрел анализ и сказал: «Ну ничего страшного, просто ты плохо кушаешь, поешь мясо — и всё пройдет». Чтобы было понятно, в распечатке анализа ни один показатель не был в норме. Компетентность доктора впечатляет!
В Одесской областной больнице зашли в детское гематологическое отделение, был дежурный врач. Он спокойно просмотрел анализ и сказал: «Ну ничего страшного, просто ты плохо кушаешь, поешь мясо — и всё пройдет». Чтобы было понятно, в распечатке анализа ни один показатель не был в норме. Компетентность доктора впечатляет!
На всякий случай, чтоб перестраховаться, отправил нас на еще один анализ крови в этой же областной Одесской поликлинике. Во время второго анализа лаборантка впечатлилась, потому что аппарат не показывал лейкоциты. Вообще не показывал. Она сказала, что в таких случаях считают через микроскоп. Мы стали ждать. Она вернулась, мы зашли, мама спросила, сколько денег мы должны. Ответ: «Вы что, с ума сошли, мы с таких больных денег не берем».
Потом была больница на Слободке. Срочная реанимация. Переливание трех пакетов крови. Диагноза всё еще нет. На следующий день гематологическое отделение. Снова анализ крови — в тот день я сдала 9 раз. Сказали лейкоз. Форма, тип — не определены.
15 декабря. Диагноз
У меня первый раз взяли пункцию костного мозга из грудины (между ребрами). Честно говоря, это адская боль. В нашей больнице мне помазали это место лидокаином. Потом ввели туда толстенную иголку, я таких еще до этого не видела. Надавила на меня эта врачиха, кровь не идет. Налегла на меня всем весом и говорит: «Расслабься». По ощущениям — как будто из тебя вынимают душу. Ну, в общем, дальше ожидание результатов анализов. И диагноз: острый лимфобластный лейкоз.
Наши врачи не стали морочить голову. Они сразу сказали, что в нашей стране эта болезнь неизлечима и является смертельной. Еще сказали, что времени у нас буквально сутки, потому что количество бластных (раковых) клеток в крови 90%.
В этот же день мы взяли билеты на самолет и полетели в Израиль.
Посадка была тяжелой, начались судороги во всем теле. Пилот долго садился. Но неприятность эту мы пережили. Прилетели в три часа ночи, отделение не работало, мы поселились в гостинице при клинике. Сон.
Сон.
16 декабря 2013 года, исследования в клинике Адасса
Здесь все по-другому. В первый день сдавала анализ крови. Говорю: «У меня свободных пальцев нет». А они: «У нас кровь из пальца уже 15 лет не берут». Ввели такую тоненькую иголочку в вену (не то что наши толстенные), а потом всё автоматически. Колбочки меняются, ничего никуда переливать не надо. В общем, это была первая мистика.
Поскольку результаты наших анализов здесь не котируются, пришлось сдавать заново все. И пункцию в том числе. Но опять же — для более точного анализа клеток пункцию тут берут из тазовой кости на бедре со стороны спины. И делают это под общим наркозом. Потом полностью анализ организма, чтоб быть уверенными в том, что химиотерапия в моем конкретном случае возможна. Здесь к любому лечению относятся очень ответственно. Лекарства в аптеке просто так вообще не продают, только с рецептом врача (даже витамины).
И вот в таком режиме первые пять дней госпитализации. После того как стали известны результаты всех исследований, доктор Гураль (мой душка, я так медведя назвала) назначил протокол лечения. При всех моих показаниях он сказал, что будем лечиться по немецкому протоколу BFM (Berlin, Frankfurt, Munster — города в Германии в которых он непосредственно разрабатывался). Первые пять дней протокола нужно было только пить таблетки, побочных эффектов особо не было. Только перемены настроения (кто знает, тот поймет).
После того как стали известны результаты всех исследований, доктор Гураль (мой душка, я так медведя назвала) назначил протокол лечения. При всех моих показаниях он сказал, что будем лечиться по немецкому протоколу BFM (Berlin, Frankfurt, Munster — города в Германии в которых он непосредственно разрабатывался). Первые пять дней протокола нужно было только пить таблетки, побочных эффектов особо не было. Только перемены настроения (кто знает, тот поймет).
13 января, 21-й день по протоколу
Суть протокола: это документ, в котором описаны все этапы лечения, от которых нельзя отступать. Мой первый протокол состоит из четырех этапов. Каждый этап — 33 дня, после которого берут анализ костного мозга и смотрят, как дело идет. Химию в капельницах дают не каждый день, т.к. она очень разрушительно влияет на весь организм в целом.
На сегодняшний день у меня 10 таблеток. И домашний режим (снимаем квартиру, т.к. один день в стационаре стоит $1200).
Последние три дня мы были госпитализированы (три дня госпитализации — $5400), так как от химии были побочные эффекты. Сначала очень разболелся живот и началась рвота (это стабильная реакция), а потом вместо еды пошла кровь (зрелище что надо). Она не останавливалась, пришлось ехать в больницу, т.к. потеря крови в моем случае — самое стремное, что только можно придумать.
Сначала очень разболелся живот и началась рвота (это стабильная реакция), а потом вместо еды пошла кровь (зрелище что надо). Она не останавливалась, пришлось ехать в больницу, т.к. потеря крови в моем случае — самое стремное, что только можно придумать.
Остановить кровотечение не могли сутки, вкололи миллион лекарств. Причина до сих пор не известна, поэтому доктора начали меня бояться. Такая вот я нетипичная баба.
Сегодня чувствую себя достаточно неплохо — усталость, слабость, раздражительность, жуткая боль в костях и голове — это теперь мое постоянное состояние и входит в понятие «неплохо» и «жить можно».
Я пока еще волосатая. Уговорила маму, сегодня маникюрными ножничками постригусь. Всю жизнь об этом мечтала! МЕЧТЫ СБЫВАЮТСЯ.
Финансовая сторона вопроса — в Израиле при лечении работает принцип: платишь, когда лечишься. Доктора не могут предугадать, какие реакции возникнут при лечении, поэтому никакие суммы не предсказуемы.
На сегодня по истечении 21 дня мы потратили (не учитывая никакие бытовые нужды, только на лечение) — $23 тыс.
14 января, 22-й день по протоколу, лечение в дневном стационаре
Отделение открывается в 8:00. К этому времени нам необходимо быть в больнице, получить свой номер (от него зависит, насколько быстро со мной начнут работать) и оплатить лечение за этот день ($1,2 тыс.)
Когда подходит моя очередь, берут анализ крови из пик-лайна (это такой катетер, через который вводят химию и все другие лекарства). По результатам анализа проверяют, какие лекарства сегодня можно вводить без угрозы для жизни. В это смысле здесь врачи очень щепетильны. В моем анализе всё было в пределах нормы, поэтому я получила всю свою химию в этот день.
Вводят ее разными способами, LD — самое стремное из всего, что только можно придумать. Благо тут всего минут 10.
Меня выкладывают на бочок, заставляют полностью сложиться, подтянуть ноги к животу а голову к ногам, для того чтобы максимально растянуть позвоночник. Потом между позвонками вкалывают анестезию, оно очень печет, но тоже терпимо. Пять минуток перерыв, чтоб обезболивающее сработало. Потом мой любимый доктор (в этот момент я перестаю его так сильно любить) вводит между позвонками иголку до того момента, пока не доберется до спинномозговой жидкости, высасывает ее оттуда шприцем, для того чтобы освободить место для химии, и вот он, этот момент! Адская боль по всему позвоночнику и голове минут пять, пока лекарство вводят, его надо вводить медленно, чтобы, не дай Бог, ноги не отказали. Здесь момент для слез и соплей, и — уфф, процедура окончена.
Пять минуток перерыв, чтоб обезболивающее сработало. Потом мой любимый доктор (в этот момент я перестаю его так сильно любить) вводит между позвонками иголку до того момента, пока не доберется до спинномозговой жидкости, высасывает ее оттуда шприцем, для того чтобы освободить место для химии, и вот он, этот момент! Адская боль по всему позвоночнику и голове минут пять, пока лекарство вводят, его надо вводить медленно, чтобы, не дай Бог, ноги не отказали. Здесь момент для слез и соплей, и — уфф, процедура окончена.
После каждого такого укола доктор очень нервничает, спрашивает, не очень ли у меня болит голова, и всегда предупреждает, что на следующий день боли могут быть невыносимые, мне сразу обезболивающее домой выписывают.
В течение еще целого часа нельзя вставать с кровати и голова должна находиться ниже уровня всего тела.
Как я уже писала, мы приходим в больницу в восемь утра, а уходим часов в пять вечера. Вот такой себе один день с стационаре. Он, конечно, не всегда проходит одинаково, потому что лекарства вводят разные и иногда возникают проблемы с тем, что лекарства в отделении нет, тогда приходится подождать, пока принесут.
В течение всего дня по больнице ходят волонтеры. Они приносят пирожные и поют песни — веселят народ, помогают в пустяках.
Дают еще обед, по мне он, конечно, жуткий… Один раз лежала в другом отделении, вот там было идеально, а тут у них с едой фу-фу-фу, хоть это чуть ли не единственный недостаток.
Что сказали доктора
Ну, во-первых, у меня их как бы два: Гураль Сашка (это мой душка-доктор, он очень внимательный и у него золотые руки, мой медведь в его честь) и доктор Вайнштейн Вова (как я его называю, доктор-живодер, он молодой, у него чешутся руки, и он не контролирует свои врачебные порывы, ему лишь бы в меня что-то вколоть, в общем, рисковый малый).
Вайнштейн, в общем, сказал, что у меня за последние дни упал белок и что мне надо больше кушать, а я только и делаю, что кушаю! Не знаю, куда еще больше. А еще сказал, что все остальные показатели не падают, что в принципе неплохо, и еще что организм плохо пока что вырабатывает новые клетки.
С горем пополам мы закончили первую часть протокола. Не обошлось без очередной госпитализации. Я умудрилась даже с повязкой поймать воспаление легких, целую неделю получала антибиотики и, соответственно, лежала в стационаре.
В тот раз, когда нас выписали, я впервые почувствовала, что изоляция лучше, чем шумный поток людей. На улице мне было так громко и светло, что я даже на пару минуту испугалась, но, слава Богу, это быстро прошло. После того как состояние стабилизировалось, мы поговорили с доктором, и он сказал, что можно продолжить курс химии. В последние две недели осложнений не было, так что речь пошла о пересадке (костного мозга). Гураль сказал, что если мама привезет Даника (младший брат Насти, ему 4 года, и он подошел как донор для пересадки. — «Известия») пораньше, то химию до конца можно будет даже не капать.
Естественно, моей радости не было предела, потому что терпеть это дело не так уж и просто, особенно третий месяц подряд, каждый день. В общем, мама сорвалась и полетела домой всего на два дня. Я осталась вдвоем с соседкой.
Я осталась вдвоем с соседкой.
Зовут ее Ира, ей 23, и у нее тоже лейкоз. Сама она из Москвы, очень позитивный человек. У нас с ней не совпадают моменты пессимизма, так что получается друг друга растормошить. Мама, впрочем, не любит наш черный юмор по поводу причесок.
Мама вернулась с Даником и бабулей, и мы снова пошли в клинику — разбираться с продолжением химии и пересадкой. Гураль залетел в отделение и сказал, что никакой химии сегодня уже не будет, я расслаблено вдохнула. Но не тут-то было… Он только предупредил, что осталось проконсультироваться с трансплантологом.
И вот через пару часов он снова приходит и говорит: «К сожалению, мы не можем остановить протокол, не закончив его. Значит, химию нужно продолжить… И еще — для того чтобы сделать пересадку, необходимо, чтобы анализ костного мозга (кровь внутри костей) был абсолютно чистый, без бластных (раковых) клеток». Получилось, что всё очень прилично растянулось по времени.
Анализ костного мозга можно делать как минимум через две недели после последней химии… Его можно делать, только когда все показатели поднимутся до минимального уровня, а химия направлена на то, чтобы эти самые показатели понизить как можно больше… в итоге мы застряли по времени.
Сдала анализ крови, почти все показатели (кроме лейкоцитов) уже в норме, будем ждать, пока и они поднимутся, для чего я получаю каждый день укол в плечо. Но это ничего, всё так привычно уже, хоть я все еще терпеть не могу эти уколы в позвоночник.
27 марта 2014 года — мне 19!
Даник тут, конечно, резвится. Все уже без него жить не могут, он всех покорил.
И, кстати, помимо всего прочего, мне уже теперь 19, что звучит гордо!
Каждый новый год теперь такое счастье! И почему только раньше это так не ценилось? Говорят же, что мы не ценим, пока не потеряем. Но кто же слушает других людей? Всё закономерно.
Больше ничего интересного в голову не приходит…
У нас — лето, +27, жара впечатляющая. Жаль, на солнце нельзя находиться, приходится гулять только утром и вечером.
В целом я себя чувствую хорошо, болит всё не так уж сильно (или я просто уже привыкла, не знаю), температуры сегодня не было, что тоже хороший признак. Единственное, что напрягает, — бессонница… Спать ложусь в пять утра, мама, конечно, переживает насчет этого, но пить снотворное и всякие дополнительные таблетки я не хочу.
…За количеством дней лечения я перестала следить давно, но, наверное, их где-то 150. Я снова принимаю химию, т.к. доктор сказал, что перед пересадкой необходимо пройти еще один курс. Анализ не совсем чистый, есть остаточные бластные клетки.
Теперь у меня пять дней госпитализации, и все 24 часа в сутки я получаю химию. Сначала тот препарат, который мне кололи в спину, а теперь другой, который дестабилизирует действие этого самого метотриксата.Чувствую себя не очень, уже второй день не ем — минус 1 кг на моем счету. Сегодня утром мама смогла заставить меня скушать завтрак, но он не продержался во мне и пяти минут. Больше она меня не заставляет. Доктор сказал, что диагностировали печеночную недостаточность. Но природу происхождения определить не могут. Все таблетки, которые я принимала раньше, отменили. Но пока что легче не становится.
4-й день химии — будто меня переехали автобусом
Ну что я вам могу сказать: «Чем дальше в лес, тем больше дров».
Чувствую себя жутко. Всё еще ничего не ела, бывает, только пью сок. За эти дни потеряла 2,5 кг. Ощущения, как будто меня переехали автобусом. Очень сильно болят кости, а особенно челюсть, я совсем мало разговариваю.
Зато показатели крови достаточно высокие. Лейкоциты 4,5 (при норме от 4 до 6). Немного низкий гемоглобин, поэтому мало сил. Сегодня гулять не выходила, а вчера смогла заставить себя выйти на минут 20 на воздух. Говорят, что надо много пить и купаться, чтоб химия быстрее выходила. И, слава Богу, в этот раз мне хочется пить всё время.
Про погоду мне даже рассказать нечего, выхожу на улицу только поздно — чтоб не жарко было и поменьше людей.
Кстати, в этот раз меня положили в трансплантологию (это отделение такое), потому что в моей гематологии не было мест. Ну и еще потому что я попросилась лечь вместе с Иркой, мы друг друга стимулируем. Выходим гулять вместе, а то сами себя заставить не можем.
Мама уже держится бодрячком.
Купила мне сок и фрукты, так что придется что-то съесть.
…Я так устала лечиться. Это обидно, когда ты себя уже нормально чувствуешь, а потом тебе снова начинают капать эту химию и ты заново не можешь ничего делать. Радует только, что на этот раз всего пять дней.
23 мая 2014 — лучше пересадка от мамы, но это дороже
После очередной консультации с доктором стало понятно, что пересадку нужно было делать еще вчера. Оказывается, что в тот момент, когда я летала домой и виделась со всеми вами, мои дорогие, я должна была уже лежать на пересадке.
После последней химии у меня очень сильно поднялись печеночные пробы (мои показатели 1340 и 1200 при норме до 30). При таких данных пересадку делать невозможно, а счет идет уже на дни. Теперь мы ждем, пока показатели придут в норму.
Из-за столь высоких показателей врачи стали подозревать рак печени, но, слава Богу, эти пробы стали падать, значит, это просто реакция организма на химию.
Также на консультации нам сказали, что пересадку можно сделать от мамы, а не только от Даника, но это стоит дороже (мы с мамой никак не можем достигнуть согласия по вопросу пересадки. Мне, конечно, тоже жалко Даника, но кажется, что он со временем все забудет. Может, конечно, и не всё, но в любом случае потрясение будет минимальным, тем более что процесс забора костного мозга у донора проходит под наркозом. Он всего лишь поспит и потом проснется. И стоит это $153 тыс. Деньги, конечно, немыслимые, но это меньше, чем при пересадке от мамы).
Врачи предупреждают, что риск для здоровья больше при пересадке от Даника, т.к. при пересадке от него в моем организме должны будут замениться все клетки, а при пересадке от мамы — только половина. Период восстановления после пересадки от Даника будет очень мучительным. Но многие с этим справляются, и я справлюсь!
Конечно, не радует только то, что времени крайне мало и время рискнуть всё ближе.
И, главное, денег на пересадку не только от мамы, но и от Даника, уже нет. Просто нет.
Деньги на лечение Насти собирает БФ «Территория совести»
ОГРН 1127799023560
ИНН 7725351520
КПП 772501001
Юридический адрес: 119334, г. Москва, 5-й Донской проезд,
д. 23, пом. VIII, ком. 38
Р/с 407 038 10152000000005
В ОАО «НОРДЕА БАНК» г. Москва
к/с 30101810900000000990
БИК 044583990
В назначение платежа просьба указать: оплата ТКМ и реабилитации Калитенко А.С. 27.03.1995 г.р.
Можно сделать пожертвование через QIWI:http://territoriya-sovesti.ru/qiwi-done
Можно пожертвовать через SMS: http://territoriya-sovesti.ru/pozhertvovat-cherez-sms
Другие способы помощи Насте здесь: http://planeta.ru/campaigns/7221
Данные для валютных переводов:
BANK NAME: OJSC NORDEA BANK MOSCOW RUSSIA
125040, MOSCOW, 3 YAMSKOGO POLE, DOM 19, STROENIE 1
SWIFT:
NDEARUMM
account: 407 038 10152000000005.
Beneficiary: Charity fund
«Territoriya Sovesti»
Address: 5 Donskoy proezd, 23, pom. VIII. 38.
119334. City/Country: Moscow, Russia. Currency in ROUBLES.
Comission:
charity.
The destination of the transfer: charity donation for the treatment of Kalitenko Anastasia, 27.03.1995.
ACCOUNT NUMBER: $ 40703840352000100005
ACCOUNT NUMBER: E 40703978952000100005
Лейкемия
Лейкемия (лейкоз) – это злокачественное изменение кроветворных органов, характеризующееся подавлением нормальной функции кроветворения, с замещением нормальных клеток пролиферацией незрелых, низкодифференцированных и ненормально работающих, активных (при остром течении) или с резким ростом количества зрелых лимфоидных клеток в крови, а также в лимфоузлах, печени и селезенке (в случае хронического течения болезни) Лейкоз может развиться вне зависимости от пола и возраста пациента. Среди причин, которые могут привести к лейкозу, выделяют химические канцерогены (ароматические углеводороды — в особенности бензол, препараты химиотерапии — цитостатики), ионизирующее излучение (в том числе лучевая терапия рака), иммунодефицитные состояния, наследственные дефекты хромосом.
Виды лейкемии
Лейкемии можно подразделить на 2 типа:
— острые лейкозы. Развиваются быстро и при отсутствии лечения приводят к резкому ухудшению состояния, вплоть до смертельного исхода. В случае своевременной диагностики и адекватного лечения прогноз благоприятный.
— хронические лейкозы. Развивается медленно, пациент с такой формой заболевания может не знать о нем в течение нескольких лет. При отсутствии лечения возможен переход в тяжело поддающиеся терапии острые формы.
По общему количеству в периферической крови лейкоцитов и наличию бластных клеток:
— лейкемические (с резким увеличением числа лейкоцитов — более, чем 50—80×109/л в периферической крови, с бластными клетками)
— сублейкемические (50—80×109/л лейкоцитов, характеризуется наличием бластных клеток)
— лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты)
— алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют)
Также стоит отметить, что при определении ферментов бластных клеток могут быть дифференцированы лимфобластные и миелобластные лейкозы.
Симптомы лейкоза
Для лейкоза характерны следующие симптомы:
— слабость, высокая утомляемость,
— анемия (снижение концентрации гемоглобина в крови),
— нарушение функции желудочно-кишечного тракта (снижение аппетита, тошнота, рвота),
— значительное повышение температуры,
— увеличение селезенки, печени и/или лимфатических узлов,
— костные боли.
При более запущенных стадиях происходит снижение массы тела и появление геморрагических симптомов – кровотечений из слизистых, точечных кровоизлияний и кровоподтеков, внутренних кровотечений. При остром течении болезни возможна лихорадка с ангиной, стоматитом и кровоточивостью.
Как диагностируется лейкемия
Заподозрить лейкоз можно при резких изменениях клеточного состава крови (так называемой гемограммы). Диагноз «лейкоз» ставится на основании изучения пунктата костного мозга (биопсию чаще всего проводят в области грудной клетки) и клинических симптомов. При наличии в костном мозге бластных клеток ставится острая форма лейкоза. Далее устанавливается подтип лейкоза — проводятся гистохимические, иммунологические и цитогенетические исследования. Иммуногистохимическое исследование позволяет установить фенотип клеток, и на его основании скорректировать стратегию лечения, а также определить прогноз.
Хроническая форма лейкоза (лимфолейкоз) первично определяется при изучении мазков периферической крови, а также при наличии увеличенной селезенки и/или лимфоузлов. При наличии абсолютного лимфоцитоза необходимо дополнительное биопсирование костного мозга (результатом гистологического исследования при подтвержденном диагнозе будет инфильтрация костного мозга зрелыми лимфоцитами).
Специализированное научно-практическое издания для ветеринарных врачей и студентов ветеринарных ВУЗов.
TogglerВыпуски журнала по годам
Контакты журналаvetpeterburg
Подпишись на новости Вы можете подписаться на нашу новостную рассылку.
Для этого нужно заполнить форму, указав ваш почтовый e-mail.
Рассылка осуществляется не более 5-6 раз в год.
Администрация сайта никогда ни при каких обстоятельствах не разглашает и не передает другим лицам данные о пользователях сайта.
Покупка бумажной версии Чтобы приобрести бумажную версию журнала необходимо оформить заказ и оплатить его онлайн.
Доставка выполняется Почтой России.
Стоимость экземпляра журнала указанна с учетом доставки.
По вопросам рассылки в другие странны обращайтесь к заместителю главного редактора: [email protected].
Предзаказ Доставка для клиник
Для ветеринарных клиник г. Санкт-Петербурга и Лен. области.
Доставка производится курьером на адрес клиники в количестве одного экземпляра.
Для оформления доставки необходимо заполнить форму. Подписка на доставку оформляется один раз и действует до тех пор, пока представитель вашей организации не подаст заявку на отмену доставки.
Оформить доставку
Диагностика острого миелоидного лейкоза | Общество лейкемии и лимфомы
Очень важен точный диагноз типа лейкемии. Точный диагноз помогает врачу до
.- Оценить, как болезнь будет прогрессировать
- Определите подходящее лечение.
Диагностика острого миелоидного лейкоза (ОМЛ) и вашего подтипа ОМЛ обычно включает серию тестов. Некоторые из этих тестов можно повторять во время и после терапии, чтобы измерить эффект лечения.
Тесты, которые ваш врач может использовать для диагностики ОМЛ
Анализы крови и костного мозга
Анализы крови и костного мозга используются для диагностики AML и подтипа AML. Изменение количества и внешнего вида клеток крови помогает поставить диагноз.
Анализы крови
Образцы крови обычно берут из вены на руке. Ваша кровь отправлена в лабораторию за
- Полный анализ крови (CBC), который подсчитывает количество эритроцитов, лейкоцитов и тромбоцитов в крови.Обычно у пациентов с ОМЛ количество эритроцитов и тромбоцитов ниже ожидаемого.
- Мазок периферической крови, который показывает наличие лейкозных бластных клеток (миелобластов). У человека с ОМЛ обычно слишком много незрелых лейкоцитов (лейкозных бластов) в крови и слишком мало зрелых лейкоцитов. Незрелые клетки не функционируют как нормальные зрелые лейкоциты.
Тесты костного мозга
Образцы клеток костного мозга получают путем аспирации и биопсии костного мозга.Тестирование костного мозга включает два этапа, которые обычно выполняются одновременно в кабинете врача или больнице
- Аспирация костного мозга для отбора жидкого образца костного мозга
- Биопсия костного мозга для удаления небольшого количества кости, заполненной костным мозгом.
Образцы костного мозга обычно берут из тазовой кости. Оба образца исследуются под микроскопом на предмет хромосомных и других изменений клеток.
Генетические тесты
Генетические тесты помогают выявить изменения (мутации) в генах или хромосомах клетки.Выявление этих конкретных изменений может помочь определить варианты лечения и прогноз пациента. Следующие тесты могут быть выполнены для изучения генов лейкозных клеток пациента
- Цитогенетический анализ (кариотипирование)
- Флуоресцентная гибридизация in situ (FISH)
- Молекулярное тестирование.
Диагностика AML
Ваш врач вместе с гематопатологом подтвердит диагноз. Гематопатолог — это специалист, который изучает заболевания клеток крови, исследуя образцы крови, клеток костного мозга и других тканей.
Диагноз AML подтверждается идентификацией:
- Бластные лейкозные клетки в образцах костного мозга
- Процент бластных клеток. Бласты обычно составляют от 1 до 5 процентов клеток костного мозга. Для диагностики ОМЛ обычно требуется наличие не менее 20 процентов бластов. Но AML также можно диагностировать, если у бластов есть хромосомные изменения, которые возникают при определенном типе AML, даже если процент бластов составляет менее 20 процентов.
- Характерные маркеры (антигены) на поверхности бластных клеток, такие как CD13 или CD33 (CD — это сокращение от «обозначения кластера»).
- Клетки на основе типов маркеров (антигенов) на поверхности клетки с использованием процесса, называемого «иммунофенотипирование (проточная цитомертизация)».
Щелкните здесь, чтобы узнать, как установить новый диагноз острого лейкоза.
Хромосомные и генные аномалии
Хромосомные изменения и генетические мутации являются важным прогностическим фактором для прогнозирования частоты ремиссии, риска рецидивов и результатов выживания. Однако не все пациенты имеют хромосомную аномалию, и пациенты могут иметь мутации генов, отличные от других пациентов с ОМЛ.Ваш врач проведет молекулярный анализ ваших клеток, чтобы определить конкретные генетические изменения. См. Информационный бюллетень LLS «Молекулярное профилирование рака» для получения дополнительной информации.
Откройте буклет «Острый миелоидный лейкоз», чтобы получить полный список хромосомных и генных аномалий.
Контрольный список недавно диагностированных
Колледж американских патологов (CAP) и Американское гематологическое общество (ASH) предоставляют практические рекомендации пациентам и лицам, осуществляющим уход за больными, с новым диагнозом острого лейкоза.Этот контрольный список поможет вам получить наилучшее лечение в вашей уникальной ситуации: Щелкните здесь
Ссылки по теме
Бластные клетки и миелобласты Обзор
В биологии и медицине суффикс «-бласт» относится к незрелым клеткам, известным как клетки-предшественники или стволовые клетки. Взрывы порождают самые разные специализированные клетки. Например, нейробласты дают начало нервным клеткам. Клетки крови происходят из бластов в костном мозге.
У всех нас есть взрывы. Фактически, мы начали как взрыв или, точнее, бластоциста (набор клеток, который делится достаточно раз, чтобы превратиться в эмбрион).
Однако, когда в неожиданных местах появляются различные типы бластов или когда развиваются аномальные бласты, они могут быть индикатором рака или другого заболевания.
ДЭВИД МАККАРТИ / Getty ImagesБластные клетки костного мозга
В здоровом костном мозге кроветворные клетки, известные как гемопоэтические стволовые клетки, превращаются в эритроциты, лейкоциты и тромбоциты в процессе, называемом кроветворением.Взаимодействие с другими людьми
Этот процесс происходит на протяжении всей вашей жизни, поскольку клетки крови постоянно образуются, чтобы заменить те, которые стали старыми или изношенными. Стволовая клетка выбирает свой путь развития в одну из двух клеточных линий, лимфоидную или миелоидную.
В линии миелоидных клеток термин «бластная клетка» относится к миелобластам или миелоидным бластам. Это самые ранние и незрелые клетки миелоидной клеточной линии.
Миелобласты дают начало лейкоцитам.Это семейство лейкоцитов включает:
- нейтрофилов
- Эозинофилы
- Базофилы и моноциты
- Макрофаги
Присутствие этих циркулирующих миелобластов может быть важным индикатором таких заболеваний, как острый миелолейкоз и миелодиспластические синдромы.
Хотя линия миелоидных клеток составляет около 85% клеток костного мозга, менее 5% должны состоять из бластных клеток. Все остальное может быть признаком серьезного заболевания.
Заболевания миелобластов
В случае острого миелогенного лейкоза (ОМЛ) и миелодиспластических синдромов (МДС) наблюдается перепроизводство аномальных миелобластов. Эти клетки не могут развиваться дальше в зрелые лейкоциты.
Острый миелолейкоз
ОМЛ — это тип рака, который имеет несколько других названий, например острый миелоцитарный лейкоз, острый миелогенный лейкоз, острый гранулоцитарный лейкоз или острый нелимфоцитарный лейкоз.Чаще всего встречается у пожилых людей.
В большинстве случаев ОМЛ развивается из клеток, которые могут превратиться в белые кровяные тельца, отличные от лимфоцитов, однако в некоторых случаях ОМЛ развивается в других типах кроветворных клеток.
Миелодиспластические синдромы
МДС — это группа заболеваний, которые влияют на выработку новых клеток крови в костном мозге. При этих заболеваниях костный мозг производит аномальные бластные клетки, которые не созревают должным образом и не могут функционировать.Взаимодействие с другими людьми
Эти аномальные бласты начинают захватывать костный мозг и препятствовать выработке достаточного количества других типов клеток крови, таких как тромбоциты, эритроциты и здоровые белые кровяные тельца.
Если производство лейкозных бластов выходит из-под контроля, они могут вылиться из костного мозга в циркулирующую кровь. Бластные клетки обычно не обнаруживаются в циркулирующей крови здоровых людей, и их присутствие в общем анализе крови (ОАК) очень подозрительно на лейкоз.Взаимодействие с другими людьми
Когда обращаться к врачу
Хотя симптомы ОМЛ и МДС на ранних стадиях часто неспецифичны, вам следует обратиться к врачу, если у вас возникнут:
- Длительное кровотечение
- Легкие синяки
- Постоянная усталость
- Частое заражение
- Необъяснимая потеря веса на 5% и более
тестов на острый миелоидный лейкоз (AML)
Определенные признаки и симптомы могут указывать на то, что у человека может быть острый миелоидный лейкоз (ОМЛ), но для подтверждения диагноза необходимы тесты.
История болезни и медицинский осмотр
Врач захочет получить подробную историю болезни , сосредоточив внимание на ваших симптомах и длительности их появления. Он или она может также спросить о других проблемах со здоровьем, а также о возможных факторах риска лейкемии.
Во время медицинского осмотра врач, скорее всего, уделит пристальное внимание вашим глазам, рту, коже, лимфатическим узлам, печени, селезенке и нервной системе и будет искать области кровотечения или синяков или возможные признаки инфекции.
Если есть основания полагать, что проблемы могут быть вызваны низким уровнем кровяных телец (анемия, инфекции, кровотечение или синяк и т. Д.), Врач, скорее всего, назначит анализы крови для проверки количества клеток крови. Также вас могут направить к гематологу, врачу, специализирующемуся на заболеваниях крови (включая лейкоз).
Типы образцов, используемых для тестирования на AML
Если врач подозревает, что у вас лейкемия, ему или ей нужно будет проверить образцы клеток вашей крови и костного мозга, чтобы убедиться в этом.Также могут быть взяты образцы других тканей и клеток, чтобы помочь в лечении.
Образцы крови
Анализы крови — это обычно первые тесты, проводимые для выявления лейкемии. Кровь берется из вены на руке.
Образцы костного мозга
Лейкемия начинается в костном мозге, поэтому проверка костного мозга на наличие лейкозных клеток является ключевой частью тестирования на нее. Образцы костного мозга берутся в результате двух анализов, которые обычно проводятся одновременно:
- Аспирация костного мозга
- Биопсия костного мозга
Образцы обычно берутся с тыльной стороны тазовой (тазовой) кости, но иногда вместо них используются другие кости.Если нужно сделать только аспирацию, ее можно взять из грудины (грудной кости).
Для аспирации костного мозга вы ложитесь на стол (на боку или на животе). Врач очистит кожу бедра, а затем обезболит эту область и поверхность кости, введя местный анестетик. Это может вызвать кратковременное покалывание или ощущение жжения. Затем в кость вводят тонкую полую иглу и с помощью шприца отсасывают небольшое количество жидкого костного мозга.Даже при использовании анестетика у большинства пациентов все еще возникают кратковременные боли при удалении костного мозга.
Биопсия костного мозга обычно выполняется сразу после аспирации. Небольшой кусок кости и костного мозга удаляется с помощью иглы чуть большего размера, которая вводится в кость. Это также может вызвать кратковременную боль. После того, как биопсия будет сделана, на это место будет оказано давление, чтобы предотвратить кровотечение.
Эти тесты костного мозга используются для диагностики лейкемии, но их также можно повторить позже, чтобы определить, реагирует ли лейкоз на лечение.
Спинномозговая жидкость
Спинномозговая жидкость (CSF) окружает головной и спинной мозг. ОМЛ иногда может распространяться на область вокруг головного и спинного мозга. Чтобы проверить это распространение, врачи могут взять образец спинномозговой жидкости для исследования (процедура называется люмбальной пункцией или спинномозговой пункцией ). Люмбальная пункция не часто используется для проверки на ОМЛ, если только у человека не наблюдаются симптомы, которые могут быть вызваны лейкозными клетками, распространившимися в головной и спинной мозг.
Для этого теста вы можете лечь на бок или сесть. Сначала врач обезболивает участок кожи в нижней части спины над позвоночником. Затем между костями позвоночника в область вокруг спинного мозга вводится небольшая полая игла, чтобы удалить часть жидкости.
Люмбальная пункция также иногда используется для доставки химиотерапевтических препаратов в спинномозговую жидкость, чтобы предотвратить или лечить распространение лейкемии в спинной и головной мозг.
Лабораторные тесты, используемые для диагностики и классификации AML
Один или несколько из следующих лабораторных тестов могут быть выполнены на образцах для диагностики AML и / или для определения конкретного подтипа AML.
Общий анализ крови и мазок периферической крови
Полный анализ крови (CBC) — это тест, который измеряет количество различных клеток в крови, таких как эритроциты, лейкоциты и тромбоциты. Общий анализ крови часто проводится вместе с дифференциалом (или разницей), который смотрит на количество различных типов белых кровяных телец. Для мазка периферической крови образец крови исследуют под микроскопом. Изменение количества и внешнего вида различных типов клеток крови часто помогает диагностировать лейкемию.
У большинства пациентов с ОМЛ в крови слишком много незрелых лейкоцитов и недостаточно эритроцитов или тромбоцитов. Многие из лейкоцитов могут быть миелобластами (часто называемыми бластами), которые представляют собой очень ранние формы кроветворных клеток, которые обычно не обнаруживаются в крови. Эти клетки не работают как нормальные зрелые лейкоциты. Эти данные могут указывать на лейкоз, но болезнь обычно не диагностируется без исследования образца клеток костного мозга.
Биохимический анализ крови и тесты на свертываемость
Эти тесты измеряют количество определенных химических веществ в крови и способность крови к свертыванию.Эти тесты не используются для диагностики лейкемии, но они могут помочь обнаружить проблемы с печенью или почками, аномальный уровень определенных минералов в крови или проблемы со свертыванием крови.
Стандартные исследования клеток под микроскопом
Образцы крови, костного мозга или спинномозговой жидкости исследуются под микроскопом патологом (врачом, специализирующимся на лабораторных исследованиях) и могут быть рассмотрены гематологом / онкологом пациента (врачом, специализирующимся на онкологических заболеваниях и заболеваниях крови).
Врачи будут изучать размер, форму и другие характеристики белых кровяных телец в образцах, чтобы классифицировать их по определенным типам.
Ключевым элементом является то, выглядят ли клетки зрелыми (как нормальные клетки крови) или незрелыми (не имеющими признаков нормальных клеток крови). Самые незрелые клетки называются миелобластами (или бластами).
Особенно важен процент бластов в костном мозге или крови. Для диагностики ОМЛ обычно требуется наличие не менее 20% бластов в костном мозге или крови. (В нормальном костном мозге количество бластов составляет 5% или меньше, тогда как кровь обычно не содержит бластов.AML также может быть диагностирован, если обнаружено (с помощью другого теста) бластные изменения хромосом, которые происходят только при определенном типе AML, даже если процент бластов не достигает 20%.
Иногда просто подсчета и просмотра клеток недостаточно для точного диагноза. Для подтверждения диагноза ОМЛ могут использоваться другие лабораторные тесты.
Цитохимия
Для цитохимических тестов клетки подвергаются воздействию химических красителей (красителей), которые вступают в реакцию только с некоторыми типами лейкозных клеток.Эти пятна вызывают изменение цвета, которое можно увидеть под микроскопом, что может помочь врачу определить, какие типы клеток присутствуют. Например, одно окрашивание может помочь отличить клетки ОМЛ от клеток острого лимфолейкоза (ОЛЛ). Окрашивание заставляет гранулы большинства клеток AML выглядеть под микроскопом в виде черных пятен, но не вызывает изменения цвета ВСЕХ клеток.
Проточная цитометрия и иммуногистохимия
И для проточной цитометрии, и для иммуноцитохимии образцы клеток обрабатывают антителами, которые представляют собой белки, которые прикрепляются только к некоторым другим белкам в клетках.Для иммуноцитохимии клетки затем исследуют под микроскопом, чтобы увидеть, прилипли ли к ним антитела (то есть они имеют эти белки), в то время как для проточной цитометрии используется специальная машина.
Эти тесты используются для иммунофенотипирования — классификации лейкозных клеток в соответствии с веществами (антигенами) на их поверхности. Клетки лейкемии могут иметь разные антигены в зависимости от того, в каком типе клеток они начинаются и насколько они зрелы, и эта информация может быть полезна при классификации AML.
Хромосомные тесты
Эти тесты исследуют хромосомы (длинные нити ДНК) внутри клеток. Нормальные клетки человека содержат 23 пары хромосом, каждая из которых имеет определенный размер и окрашивается определенным образом. Клетки AML иногда имеют хромосомные изменения, которые можно увидеть под микроскопом или обнаружить с помощью других тестов. Признание этих изменений может помочь идентифицировать определенные типы AML и может иметь важное значение для определения прогноза пациента.
Cytogenetics: В этом тесте клетки исследуются под микроскопом, чтобы увидеть, есть ли какие-либо аномалии в хромосомах.Недостатком этого теста является то, что он обычно занимает от 2 до 3 недель, потому что клетки должны расти в лабораторных чашках в течение нескольких недель, прежде чем их хромосомы можно будет увидеть.
Результаты цитогенетического тестирования записываются в сокращенной форме, описывающей хромосомные изменения:
- Транслокация означает, что части двух хромосом поменялись местами друг с другом. Например, если в хромосомах 8 и 21 местами поменялись местами, это будет записано как t (8; 21).
- Инверсия , записанная как inv (16), например, означает, что часть хромосомы 16 теперь находится в обратном порядке, но все еще прикреплена к хромосоме.
- Делеция , записанная как del (7) или -7, например, указывает на потерю части хромосомы 7.
- Добавление или дупликация , например, +8, означает, что вся хромосома 8 или ее часть была дублирована, и слишком много ее копий найдено в клетке.
Не все хромосомные изменения можно увидеть под микроскопом. Эти изменения часто можно обнаружить с помощью других лабораторных тестов.
Флуоресцентная гибридизация in situ (FISH): Этот тест более внимательно изучает клеточную ДНК с использованием специальных флуоресцентных красителей, которые прикрепляются только к определенным генам или частям определенных хромосом. FISH может обнаружить хромосомные изменения (например, транслокации), которые видны под микроскопом в стандартных цитогенетических тестах, а также некоторые изменения, которые слишком малы, чтобы их можно было увидеть при обычном цитогенетическом тестировании.
FISH можно использовать для поиска изменений в определенных генах или частях хромосом. Его можно использовать для анализа обычных образцов крови или костного мозга без предварительного выращивания их в лаборатории. Это означает, что результаты часто доступны быстрее, чем при регулярном цитогенетическом тестировании.
Полимеразная цепная реакция (ПЦР): Это очень чувствительный тест, который также может обнаружить, что некоторые изменения генов и хромосом слишком малы, чтобы их можно было увидеть под микроскопом. Это полезно для обнаружения изменений генов, которые есть только в нескольких клетках, что делает его полезным для обнаружения небольшого количества лейкозных клеток в образце (например, после лечения).
Прочие молекулярно-генетические тесты
Другие, более новые типы лабораторных тестов также могут быть выполнены на образцах для поиска определенного гена или других изменений в лейкозных клетках.
Визуальные тесты для AML
Визуализирующие тесты используют рентгеновские лучи, звуковые волны, магнитные поля или радиоактивные частицы для создания изображений внутренней части тела. Лейкоз обычно не образует опухоли, поэтому визуализирующие обследования не всегда помогают при постановке диагноза. Когда визуализирующие тесты проводятся у людей с ОМЛ, чаще всего это делается для выявления инфекций или других проблем, а не для поиска самой лейкемии.В некоторых случаях могут проводиться визуализирующие обследования, чтобы определить степень заболевания, если предполагается, что оно распространилось за пределы костного мозга и крови.
Рентгеновские снимки
Обычный рентген грудной клетки может быть выполнен при подозрении на легочную инфекцию.
Компьютерная томография (КТ)
Компьютерная томография использует рентгеновские лучи для получения подробных изображений поперечного сечения вашего тела. Этот тест может помочь определить, увеличены ли какие-либо лимфатические узлы или органы в вашем теле. Обычно это не требуется для диагностики ОМЛ, но это может быть сделано, если ваш врач подозревает, что лейкемия растет в каком-либо органе, например селезенке.
Игольная биопсия под контролем КТ: В некоторых случаях КТ может использоваться для ввода иглы для биопсии в подозреваемую аномалию, такую как абсцесс. Для этой процедуры вы ложитесь на стол для КТ-сканирования, пока врач проводит иглу для биопсии через кожу к образованию. КТ повторяется до тех пор, пока игла не окажется внутри массы. Затем образец удаляется и отправляется в лабораторию для изучения под микроскопом.
ПЭТ / КТ: Некоторые аппараты сочетают компьютерную томографию с ПЭТ-сканированием (ПЭТ / КТ-сканирование).Для сканирования ПЭТ в кровь вводят глюкозу (форма сахара), содержащую радиоактивный атом. Поскольку раковые клетки в организме быстро растут, они поглощают большое количество радиоактивного сахара. Затем специальная камера может создать изображение радиоактивных участков тела. С помощью ПЭТ / КТ-сканирования врач может сравнить области с более высокой радиоактивностью на ПЭТ-сканировании с более подробным изображением этой области на компьютерной томографии.
Магнитно-резонансная томография (МРТ)
Как и компьютерная томография, магнитно-резонансная томография позволяет получать подробные изображения мягких тканей тела.Но при МРТ вместо рентгеновских лучей используются радиоволны и сильные магниты.
МРТочень полезны при изучении головного и спинного мозга, но обычно они не нужны людям с ОМЛ.
УЗИ
Ультразвук использует звуковые волны и их эхо для получения изображений внутренних органов или образований.
Ультразвук можно использовать для осмотра лимфатических узлов у поверхности тела или для поиска увеличенных лимфатических узлов или органов, таких как печень, селезенка и почки, изнутри брюшной полости.(Его нельзя использовать, чтобы заглянуть внутрь грудной клетки, потому что ребра блокируют звуковые волны.) Иногда его используют, чтобы направить иглу биопсии в увеличенный лимфатический узел.
Острый миелоидный лейкоз (ОМЛ) | Апластическая анемия и MDS International Foundation
Острый миелоидный лейкоз (AML) — это рак крови. Это происходит, когда молодые аномальные белые кровяные тельца, называемые бластами (лейкозными клетками), начинают заполнять костного мозга , препятствуя нормальному производству крови.Врачи диагностируют ОМЛ, когда 20 из каждых 100 лейкоцитов в костном мозге составляют бластных клеток . ОМЛ является наиболее распространенным острым лейкозом, поражающим взрослых, ежегодно диагностируется около 20 000 новых случаев.
Когда люди болеют AML, взрывы быстро копируют самих себя. Это замедляет выработку эритроцитов и тромбоцитов, вызывая усталость от анемии и риск кровотечения из-за низкого уровня тромбоцитов . Также существует повышенный риск заражения, поскольку белые кровяные тельца, борющиеся с инфекцией, не созревают и не могут бороться с инфекцией.
AML также известен как острый миелогенный лейкоз , острый миелобластный лейкоз и острый нелимфоцитарный лейкоз.
Отношение к недостаточности костного мозга заболевания:
Со временем около одной трети всех случаев МДС превращается в ПОД. Риск развития ОМЛ во многом зависит от того, какой подтип МДС у вас есть на момент постановки диагноза.
- У пациента с МДС низкого риска вероятность развития ОМЛ составляет до 2 из 10.
- У пациента с МДС высокого риска вероятность развития ОМЛ составляет более 4 из 10.
У меньшего числа людей с апластической анемией и ПНГ развивается ОМЛ.
Наличие в кровообращении более высокого процента бластов, чем костный мозг: клинические последствия миелодиспластического синдрома и острых лимфоидных и миелоидных лейкозов
Корреляция процентов бластов с лабораторными характеристиками
Характеристики 2201 последовательного пациента, которые соответствовали критериям включения и были включены в результаты исследования представлены в таблице 1.Все пациенты получали схемы, содержащие ара-С и / или идарубицин, с флударабином и топотеканом или без них. Незначительные различия в терапии не привели к значительному различию результатов между терапевтическими группами (регрессионный анализ Кокса; P = 0,31 для AML, 0,81 для MDS и 0,08 для ALL).
Таблица 1 Характеристики пациентовВо всех четырех группах заболеваний у большинства пациентов процент бластов в BM был выше, чем в PB. Однако 341 (26%) из 1314 пациентов с ОМЛ, 58 (13%) из 446 пациентов с МДС, 35 (9%) из 385 пациентов с ОЛЛ и 2 (3%) из 58 пациентов с ХММЛ имел более высокий процент взрыва в PB, чем в BM.В результате небольшого числа пациентов с CMML с более высоким процентом бластов в PB, чем в BM, эта группа не была включена в последующие анализы.
В таблице 2 показаны корреляции лабораторных переменных с процентами взрывов PB и BM, а также показано, какие уровни варьировались в соответствии с относительными процентами взрывов в PB и BM. У пациентов с AML процент бластов PB значительно коррелировал с количеством лейкоцитов (WBC), абсолютным количеством лимфоцитов, а также уровнями лактатдегидрогеназы (LDH) и B2M.Пациенты с MDS и AML с более высоким процентом бластов в PB, чем в BM, имели значительно более высокие уровни лейкоцитов, абсолютное количество лимфоцитов и уровни LDH и B2M. Среди пациентов с ОЛЛ у пациентов с более высоким процентом бластов в PB, чем в BM, также было значительно более высокое абсолютное количество лимфоцитов и лейкоцитов.
Таблица 2 Лабораторные переменные при AML, MDS и ALL: корреляция с процентом бластов в PB и BM и связь с относительным процентом бластов (PB> BM blast% vs BM> PB blast%)PB бластов и выживаемость
В первоначальном одномерном анализе выживаемости мы изучили большинство известных релевантных факторов, включая цитогенетический статус, статус работоспособности, AHD, возраст, уровень ЛДГ, количество тромбоцитов, уровень B2M, абсолютное количество лимфоцитов и процент бластов только для PB и только для BM. , а также наличие более высокого процента взрыва в ПБ, чем в БМ.Только значимые ассоциации перечислены в таблице 3. У пациентов с МДС общая выживаемость была связана с цитогенетическим статусом, рабочим статусом, AHD, возрастом, уровнем ЛДГ, количеством тромбоцитов, Международной системой оценки прогнозов (IPSS) и уровнем B2M. Пациенты с МДС, у которых процент бластов в ПБ был выше, чем в БМ, имели значительно более короткую выживаемость (Таблица 3; Рисунок 1). Количество лейкоцитов не было связано с выживаемостью у пациентов с МДС. Хотя процент бластов в PB был связан с выживаемостью, процент бластов в BM, если рассматривать отдельно, не был: медиана общей выживаемости составила 9.7 месяцев для пациентов с бластами <10% BM и 10,1 месяца для пациентов с 10–20% бластов BM.
Таблица 3 Одномерный анализ выживаемости у пациентов с МДС, ОЛЛ и ОМЛ a Рисунок 1Выживаемость пациентов с МДС в соответствии с относительным процентом бластов в PB и BM. Показатели выживаемости были значительно ниже у пациентов с более высоким процентом бластов в PB, чем в BM. (Показано количество умерших / общее количество пациентов.)
У пациентов с ОЛЛ выживаемость была связана с цитогенетическим статусом, функциональным статусом, количеством лейкоцитов, абсолютным количеством лимфоцитов, возрастом, количеством тромбоцитов и уровнем B2M (таблица 3).Подобно пациентам с МДС, ВСЕ пациенты с более высоким процентом бластов в PB, чем в BM, также имели значительно более короткую выживаемость (Таблица 3; Рисунок 2). Однако ни процент бластов PB, ни BM не были связаны с выживаемостью (таблица 3).
Рисунок 2Выживаемость пациентов с ОЛЛ в зависимости от относительного процента бластов в PB и BM. Показатели выживаемости были значительно ниже у пациентов с более высоким процентом бластов в PB, чем в BM. (Показано количество умерших / общее количество пациентов.)
В группе AML общая выживаемость была связана с цитогенетическим статусом, рабочим статусом, AHD, возрастом, уровнем LDH, количеством тромбоцитов и уровнем B2M (Таблица 3). Наличие более высокого процента бластов в PB, чем в BM, не было связано с выживаемостью, несмотря на тот факт, что процент бластов как PB, так и BM, если рассматривать их индивидуально, были (Таблица 3; Рисунок 3).
Рисунок 3Выживаемость пациентов с AML в зависимости от относительного процента бластов в PB и BM.Выживаемость существенно не различалась между пациентами с более высоким процентом бластов в ПБ, чем в ВМ, и пациентами с более высоким процентом бластов в ВМ, чем в ПБ. (Показано количество умерших / общее количество пациентов.)
В многомерной модели, включающей все факторы, которые оказались значимыми при однофакторном анализе, цитогенетический статус и наличие более высокого процента бластов в PB, чем в BM, были сохранены в качестве независимого прогноза. показатели в МДС (таблица 4). Кроме того, многомерный анализ, включающий классификацию IPSS и наличие более высоких бластов в PB, чем в BM, показал, что оба показателя не зависят друг от друга в прогнозировании выживаемости.При ОЛЛ только наличие более высокого процента бластов в PB, чем в BM, было независимо связано с выживаемостью. При AML только процент взрыва в PB и BM не был независимым прогностическим фактором.
Таблица 4 Многомерный анализ факторов, связанных с более короткой выживаемостью у пациентов с МДС и ВСЕХ пациентовОбъяснение распространенных заблуждений о лейкемии
Более 62000 человек в США ежегодно заболевают лейкемией, тяжелым раком крови, который вырабатывается костным мозгом. аномальные клетки.
Лейкемия, название, производное от греческого слова «белая кровь», представляет собой рак клеток крови, который начинается в костном мозге, губчатой ткани внутри наших костей, которая служит фабрикой клеток крови в нашем организме. Когда у пациента лейкемия, аномальные незрелые лейкоциты (так называемые бласты) бесконтрольно размножаются, заполняя костный мозг и препятствуя выработке других клеток, важных для выживания, а именно эритроцитов и тромбоцитов. Это приводит к инфекциям, анемии и аномальному кровотечению.Затем бласты выходят из костного мозга в кровоток, лимфатические узлы, селезенку и мозг.
Хотя это один из самых распространенных видов рака, диагностируемых в мире (по оценкам, 350 000 случаев во всем мире в 2012 году), существует несколько популярных заблуждений о лейкемии. Читайте дальше, чтобы узнать больше об этом сложном раке крови.
1) Лейкемия — это всего лишь одно заболевание
Лейкемия — это разнообразная группа рака крови, которую можно разделить на четыре основных типа в зависимости от типа пораженных лейкоцитов и скорости их развития.Обычно костный мозг производит незрелые клетки крови, которые могут стать миелоидными стволовыми клетками или лимфоидными стволовыми клетками. Острый лейкоз возникает, когда эти клетки костного мозга не могут созреть должным образом. При хроническом лейкозе белые кровяные тельца могут частично созревать, но не борются с инфекцией так же хорошо, как нормальные белые кровяные тельца.
Острый лимфобластный лейкоз (ALL) возникает, когда слишком много стволовых клеток становятся аномальными лимфоцитами. Эти лейкозные клетки быстро проникают в организм, распространяясь на лимфатические узлы, печень, селезенку и центральную нервную систему (головной и спинной мозг).
Острый миелогенный лейкоз (AML) возникает, когда слишком много миелоидных стволовых клеток становятся незрелыми клетками крови, называемыми миелобластами. В некоторых случаях ОМЛ также может привести к тому, что слишком много стволовых клеток превратятся в аномальные клетки крови или тромбоциты. Эти взрывы вытесняют здоровые клетки костного мозга и быстро распространяются на другие части тела, включая лимфатические узлы, селезенку и мозг.
Хронический лимфобластный лейкоз (ХЛЛ) начинается в клетках, которые становятся лимфоцитами, но это медленнорастущий рак, и многие люди не имеют симптомов в течение нескольких лет.
Хронический миелоидный лейкоз (ХМЛ) начинается в ранних миелоидных клетках и прогрессирует медленнее по сравнению с острой версией. Обычно он поражает пожилых людей и редко поражает детей раннего возраста.
Острый миелоидный лейкоз — это рак, поражающий миелоидную ткань (костный мозг), в частности, предшественники лейкоцитов (миелобласты, обозначенные желтовато-коричневым цветом), которые образуют тип лейкоцитов, известный как гранулоциты.
2) Это только детский рак
Несмотря на то, что лейкемия является одним из наиболее распространенных видов рака у детей (около 30 процентов всех детских онкологических заболеваний), заболевание чаще всего возникает у пожилых людей.По данным Национального института рака, лейкемия чаще всего диагностируется у людей в возрасте от 65 до 74 лет. Распространенность различных типов лейкозов варьируется в зависимости от возрастных групп:
Острый лимфобластный лейкоз — наиболее распространенный тип лейкемии у детей.
Острый миелоидный лейкоз — наиболее распространенный тип острого лейкоза у взрослых.
Хронический миелолейкоз редко встречается у детей и обычно встречается у взрослых.
3) Лейкоз неизлечим
В последние годы прогресс в лечении хронического лейкоза стремительно прогрессирует.В 2015 году Американское общество клинических онкологов назвало новые методы лечения ХЛЛ «успехом года». В США у взрослых с хроническим лейкозом пятилетняя выживаемость составляет примерно от 60 до 80 процентов.
Однако существует острая необходимость в более совершенных методах лечения острого лейкоза. По сравнению с другими формами лейкемии пациенты с ОМЛ имеют самую низкую пятилетнюю выживаемость — примерно 25 процентов. Что касается взрослых с ОЛЛ, у 80–90 процентов пациентов будет ремиссия в той или иной форме, но примерно у половины произойдет рецидив, а общий показатель излечения составит 40 процентов.Для взрослых пациентов с рецидивом или рефрактерным (невосприимчивым) ОЛЛ пятилетняя общая выживаемость была менее 10 процентов.
Хотя новые методы лечения требуют времени, исследователи делают важные шаги вперед в разработке новых методов лечения острого лейкоза. В 2015 году в разработке находилось более 106 методов лечения лейкемии, поскольку ученые расширяют границы, чтобы нацелить рак на клеточном и молекулярном уровне. Химиотерапия является основным методом лечения лейкемии, но также используются биологические и таргетные методы лечения и трансплантация стволовых клеток.
Узнайте, как лейкемия подразделяется на стадию и степень
Стадии большинства видов рака основаны на размере и распространении опухолей. Однако, поскольку лейкоз уже возникает в развивающихся клетках крови в костном мозге, стадия лейкемии немного отличается. Стадии лейкемии часто характеризуются подсчетом клеток крови и накоплением лейкозных клеток в других органах, таких как печень или селезенка. Принятие обоснованного решения о лечении начинается со стадии или прогрессирования заболевания.Стадия лейкемии — один из наиболее важных факторов при выборе вариантов лечения. Факторы, влияющие на стадию лейкоза и прогноз, включают:
- Количество лейкоцитов или тромбоцитов
- Возраст (пожилой возраст может отрицательно повлиять на прогноз)
- История перенесенных заболеваний крови
- Хромосомные мутации или аномалии
- Повреждение костей
- Увеличенная печень или селезенка
Острый лимфолейкоз (ОЛЛ) стадии
Система пронумерованных стадий используется для описания большинства типов рака и их распространения по телу.Обычно оценивается размер опухоли и распространение рака и назначается стадия. Для ОЛЛ стадирование не происходит таким образом, потому что заболевание возникает в костном мозге и обычно не образует опухолевые массы. Поскольку ОЛЛ, скорее всего, распространится на другие органы до того, как он будет обнаружен, метод определения стадии должен учитывать другие факторы, помимо распространения, чтобы дифференцировать стадии.
Вместо того, чтобы использовать традиционные методы определения стадии, врачи часто учитывают подтип ОЛЛ и возраст пациента.Обычно это включает цитологические тесты, проточную цитометрию и другие лабораторные тесты для определения подтипа ОЛЛ.
B-клетка ВСЕ стадия
В костном мозге вырабатываетсяВ-лимфоцитов или В-клеток. Они там тоже взрослеют. В-клетки играют большую роль в гуморальном иммунном ответе и выполняют основные функции по выработке антител против антигенов и превращаются в В-клетки памяти после того, как они были активированы взаимодействием антигенов.
- Раннее ВСЕ до Б: примерно 10% ВСЕХ случаев
- Обычный ВСЕ: примерно в 50% случаев
- Pre-B ALL: примерно в 10% случаев
- Зрелые В-клетки ВСЕ: примерно 4% случаев
ВСЕ стадия Т-клеток
Т-лимфоцитов, или Т-клеток, покидают костный мозг до созревания и перемещаются в тимус, где созревают.Т-клетки играют центральную роль в клеточном иммунитете. Есть несколько разных подмножеств Т-клеток, которые выполняют разные функции. Различные подмножества Т-клеток включают хелперные, цитотоксические, запоминающие, регулирующие, естественные киллеры и гамма-дельта-Т-клетки.
- Pre-T ALL: примерно от 5 до 10 процентов случаев
- Зрелые Т-лимфоциты ALL: примерно от 15 до 20 процентов случаев
Острый миелолейкоз (ОМЛ) стадии
Поскольку ОМЛ начинается в костном мозге и обычно не обнаруживается до тех пор, пока не распространился на другие органы, традиционное определение стадии рака не требуется.Вместо использования обычного метода TNM для оценки рака подтип AML классифицируется с использованием цитологической (клеточной) системы. Врачи могут лучше предсказать реакцию рака на лечение на основе клеточной классификации и, в свою очередь, более точно оценить прогноз.
Подтипы и стадия ОМЛ
Используя систему, известную как французско-американо-британская (FAB) классификация, AML классифицируется на восемь подтипов, от M0 до M7, на основе:
- Количество здоровых клеток крови
- Размер и количество лейкозных клеток
- Изменения, которые появляются в хромосомах лейкозных клеток
- Любые другие произошедшие генетические аномалии
Восемь этапов ПОД классифицируются следующим образом:
- Недифференцированный ОМЛ — M0: На этой стадии острого миелогенного лейкоза клетки костного мозга не обнаруживают значимых признаков дифференцировки.
- Миелобластный лейкоз — M1: Клетки костного мозга обнаруживают некоторые признаки гранулоцитарной дифференцировки с минимальным созреванием клеток или без него.
- Миелобластный лейкоз — M2: Созревание клеток костного мозга превышает стадию промиелоцитов (ранних гранулоцитов). Может наблюдаться различное количество созревания гранулоцитов.
- Промиелоцитарный лейкоз — M3: Большинство аномальных клеток представляют собой ранние гранулоциты, находящиеся между миелобластами и миелоцитами на стадии их развития.Клетки содержат множество мелких частиц и имеют ядра разного размера и формы.
- Миеломоноцитарный лейкоз — M4: На этой стадии острого миелогенного лейкоза в костном мозге и циркулирующей крови содержится различное количество моноцитов и дифференцированных гранулоцитов. Процент моноцитов и промоноцитов в костном мозге превышает 20 процентов. Также может быть повышенное количество гранулярных лейкоцитов, называемых эозинофилами, типом гранулоцитов, которые часто имеют двухлепестковое ядро.
- Моноцитарный лейкоз — M5: Эта подгруппа делится на две разные категории. Для первого характерны плохо дифференцированные монобласты с ажурным генетическим материалом. Вторая подгруппа характеризуется большим количеством монобластов, промоноцитов и моноцитов. Доля моноцитов в кровотоке может быть выше, чем в костном мозге.
- Эритролейкоз — M6: Эта форма лейкемии характеризуется аномальными клетками, образующими эритроциты, которые составляют более половины ядерных клеток в костном мозге.
- Мегакариобластный лейкоз — M7 : Бластные клетки при этой форме лейкемии выглядят как незрелые мегакариоциты (гигантские клетки костного мозга) или лимфобласты (лимфоцитообразующие клетки). Лейкоз M7 можно отличить по обширным отложениям фиброзной ткани (фиброзу) в костном мозге.
Хронический лимфолейкоз (ХЛЛ) стадии
Из-за того, как это заболевание развивается и распространяется, стадирование ХЛЛ отличается от стадии рака, который формирует опухоли.Вместо того, чтобы оценивать размер и степень опухолей, система определения стадии Rai основана на подсчете клеток крови. Система Бине (более широко используемая в Европе, чем в Соединенных Штатах) суммирует распространение рака по лимфатическим узлам на трех стадиях, просто обозначенных A, B и C. чтобы начать лечение и определить, какие методы лечения ХЛЛ могут быть наиболее эффективными для вас.
Промежуточная система Rai для CLL
Стадии хронического лимфолейкоза в системе Rai определяются тремя основными факторами: количеством лимфоцитов в крови; увеличены ли лимфатические узлы, селезенка или печень; и развились ли заболевания крови: анемия (слишком мало эритроцитов) или тромбоцитопения (слишком мало тромбоцитов).
В общем, ХЛЛ начинается как состояние, называемое лимфоцитозом, при котором слишком много лимфоцитов. Количество более 10 000 лимфоцитов в образце считается слишком высоким и является эталоном для стадии 0. Пять стадий помечены римскими цифрами 0-IV:
.- Раи ХЛЛ стадии 0: Уровни лимфоцитов слишком высоки, обычно более 10 000 в одном образце. На данный момент никаких других симптомов не развилось, и количество других клеток крови в норме.
- Rai, Стадия I ХЛЛ: Помимо высокого уровня лимфоцитов (лимфоцитоз), увеличиваются лимфатические узлы.Уровни эритроцитов и тромбоцитов все еще в норме.
- Rai, стадия II CLL: количество лимфоцитов остается высоким, и теперь печень или селезенка могут быть больше, чем обычно.
- Rai CLL Стадия III: Избыточное количество лимфоцитов начинает вытеснять эритроциты, что приводит к анемии. Лимфатические узлы могут увеличиваться, а печень или селезенка могут быть больше, чем обычно.
- Rai CLL Стадия IV: Уровни эритроцитов и тромбоцитов падают ниже нормы, вызывая анемию и тромбоцитопению.Лимфатические узлы могут увеличиваться, а печень или селезенка могут быть больше, чем обычно.
Систему Rai для определения стадии хронического лимфоцитарного лейкоза иногда упрощают до категорий низкого (стадия 0), среднего (стадии I и II) и высокого (стадии III и IV) риска. Врачи могут использовать эту классификацию, чтобы определить, когда начинать лечение.
Ступенчатая система Binet
Подобно системе Rai, поздние стадии хронического лимфолейкоза характеризуются наличием заболеваний крови, возникающих из-за недостаточного количества эритроцитов и тромбоцитов.Однако вместо того, чтобы полагаться на результаты анализа крови, система Бине оценивает, сколько участков лимфоидной ткани поражено. (Примечание: стадии Бине обычно называют клинической стадией.)
- Клиническая стадия A: лимфатические узлы могут увеличиваться, но рак ограничен менее чем тремя областями.
- Клиническая стадия B: опухло более трех участков лимфоидной ткани.
- Клиническая стадия C. Развивается одно или оба заболевания крови — анемия и тромбоцитопения.
Хронический миелолейкоз стадии
Чтобы определить стадию ХМЛ, ваш врач проверит анализы крови и костного мозга, чтобы определить количество больных клеток.

 Цитохимия и электронная микроскопия клеток крови и кроветворных органов. Киев: Наук думка, 1974. 248 с.
Цитохимия и электронная микроскопия клеток крови и кроветворных органов. Киев: Наук думка, 1974. 248 с. Москва: РОНЦ, 2003. 42 с.
Москва: РОНЦ, 2003. 42 с. TAL1 expression does not occur in the majority of T-ALL blasts. Br J Haematol 1998; 102: 440.
TAL1 expression does not occur in the majority of T-ALL blasts. Br J Haematol 1998; 102: 440.